زينون
هذه المقالة بحاجة لمراجعة خبير مختص في مجالها. (مايو 2016) |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المظهر | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
غاز عديم اللون، ذو وميض أزرق في حالة البلازما الخطوط الطيفية للزينون | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الخواص العامة | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الاسم، العدد، الرمز | زينون، 54، Xe | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| تصنيف العنصر | غاز نبيل | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المجموعة، الدورة، المستوى الفرعي | 18، 5، p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الكتلة الذرية | 131.293 غ·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| توزيع إلكتروني | Kr]; 5s2 4d10 5p6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| توزيع الإلكترونات لكل غلاف تكافؤ | 2, 8, 18, 18, 8 (صورة) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الخواص الفيزيائية | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الطور | غاز | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الكثافة | (0 °س، 101.325 كيلوباسكال) 5.894 غ/ل | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| كثافة السائل عند نقطة الغليان | 3.057[1] غ·سم−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة الانصهار | (101.325 كيلوباسكال) 161.4 ك، −111.7 °س، −169.1 °ف | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة الغليان | (101.325 كيلوباسكال) 165.03 ك، −108.12 °س، −162.62 °ف | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة ثلاثية | 161.405 كلفن (-112°س)، 81.6[2] كيلوباسكال | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| النقطة الحرجة | 289.77 ك، 5.841 ميغاباسكال | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارة الانصهار | (101.325 كيلوباسكال) 2.27 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارة التبخر | (101.325 كيلوباسكال) 12.64 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| السعة الحرارية (عند 25 °س) | 100 كيلوباسكال, 20.786 جول·مول−1·كلفن−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ضغط البخار | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الخواص الذرية | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| أرقام الأكسدة | 0, +1, +2, +4, +6, +8 (نادراً مايكون غير الصفر) (وفي حال غير ذلك فإن أكاسيده حمضية ضعيفة) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الكهرسلبية | 2.6 (مقياس باولنغ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| طاقات التأين | الأول: 1170.4 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الثاني: 2046.4 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الثالث: 3099.4 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر تساهمي | 9±140 بيكومتر | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر فان دير فالس | 216 بيكومتر | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| خواص أخرى | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| البنية البلورية | مكعب مركزي الوجه | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المغناطيسية | مغناطيسية معاكسة[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الناقلية الحرارية | 5.65×10-3 واط·متر−1·كلفن−1 (300 كلفن) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سرعة الصوت | (سائل) 1090 ، (غاز) 169 متر/ثانية | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رقم CAS | 7440-63-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| النظائر الأكثر ثباتاً | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المقالة الرئيسية: نظائر الزينون | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
الزينون (بالإنجليزية:Xenon) عنصر كيميائي رمزه Xe ورقم ذري 54 في الجدول الدوري، كتلته الذرية 131.293 جرام/مول، رقمه الدوري 5، حالته القياسية غاز عند درجة حرارة 298 كلفن.[4][5][6] هذا العنصر غاز نبيل ثقيل لا لون ولا رائحة له. يوجد في الغلاف الجوي للأرض (بكميات قليلة جدا على هيئة مقادير خطية رغم أنه ليس له رد فعل عامة، يستطيع تحمل بعض التفاعلات الكيميائية كتركيب سداسي فلورو بلاتينات الزينون (Xenon hexafluoroplatinate) أول غاز نبيل مركب يمكن تركيبه. عنصر الزينون الموجود طبيعيا يتكون من تسعة نظائر مستقرة. هناك أيضا أكثر من 40 نظير غير مستقر تخضع للتحلل الإشعاعي. تعد نظائر الزينون وسيلة هامة لدراسة تاريخ النظام الشمسي. زينونن-135 ينتج عن الانشطار النووي ويعمل كماص للنيوترونات في المفاعلات النووية. يستعمل الزينون في مصابيح الفلاش والمصابيح المقوسة وكذا التبنيج أو التخدير العام كما أن أول نموذج ليزر إكسيمر استعمل جزيء زينون ثنائ الوحدات (Xe2) كوسيط ليزري.
تاريخ
[عدل]تم اكتشاف عنصر «زينون» في إنجلترا من قبل ويليام رامزي وموريس كرافرس في 12 جويلية 1898 فقط بعد اكتشافهما للعنصرين«كريبتون والنيون» لهذا الغاز. وجداه في البقايا المتبخرة لعناصر سائل جوي. اقترح رامساي اسم «زينون» لهاذ الغاز من الكلمة اليونانية xenon مفردها xenes الذي يعني غريب أو ضيف في سنة 1902 توقع رامساي أن جزء من «زينون» في جو الأرض هو 1 من 20 مليون. خلال الثلاثينيات من القرن الماضي المهندس هارولد ادجرتون بدا في بحث تكنولوجيا الضوء strbe للتصوير العالي السرعة. أدى هذا به إلى اختراع المصباح الوامض المشغل بعنصر «زينون» الذي ينتج الضوء بإرسال تيار كهربائي سريع عبر أنبوب مليء بغاز «زينون» في 1934. ادجرتون كان قادرا على إنتاج ومضات قصيرة كجزء صغير من الثانية مايكرو ثانية بهذه الطريقة. في 1939 بدأ البرت وجوفير يبحث عن أسباب السكر للغطاسين في عمق البحر. اختبر التأثيرات المتنوعة الأمزجة المستنشقة على مواضيعه واكتشف أن ذلك سبب للغطاسين تغيرا عن الولوج في العمق. من خلال نتائجه استنتج ان غاز «زينون» يمكن استعماله كمخدر. رغم أن لزهراف في روسيا على ما يبدو درس تخدير غاز «زينون» في 1941 أول تقري منشور يؤكد التخدير بغاز «زينون» كان في 1946 من قبل ج.ه لورانس الذي جرب واختبر على الفئران. استعمل عنصر «زينون» لأول مرة كمخدر للجراحة في 1951 من طرف ستيوارت. كالن الذي أجري عمليات جراحية ناجحة على مريضين. عنصر «زينون» والغازات النبيلة الأخرى اعتبروا المدة طويلة أنهم كيميائيا وغير قادرة على التركيب أو إنتاج عناصر مركبة. لكن خلال التدريس في جامعة كولومبيا بريتش، اكتشف بارتلر ان غاز بلاتينيوم هيكسافلوريد (ptf6) عبارة عن عنصر أوكسيديزين قوي يستطيع أكسدة غاز الأكسجين O2 لتشكيل أو تركيب ديو كسجنيل هيكسا فيلوربلاتينات ((ptf6) O2.بما أن O2 و«زينون» لهما تقريبا نفس القدرة الأيونية الأولى، بارتلر تحقق أو استخلص أن بلاتين يوم هيكسافلوريد ربما يمكنه أيضا أكسدة «زينون». في 23 مارس 1962 اعتقد بارتلر أن تركيبته تكون (ptf6) X2. رغم أن عمله فيما بعد اكد احتمال كبير أن يكون مزيجا من عدة عناصر «زينون» تحتوي على أملاح. من ثم مركبات زينونية أخرى تم اكتشافها سويا مع بعض مركبات من غازات نبيلة. أرغون كريبتون رادون. إضافة إلى أرغون فليروهيديد (HA1F) كريبتون ديفيليوريد (K1 F2) واردون فليوريد حوالي سنة 1971 أكثر من 80 عنصر زينوني مركب تم التعرف عليها. في 1960 اكتشف الفيزيائي جون رينولدز أن أجزاء من نيازك احتوت على كميات غزيرة من نظائر شاذة في التركيبة من النظير زينون-129 واستنتج ان هذه الكمية هي ناتج اضمحلال للنظير المشع يود-129. نتج هذا النظير ببطء بواسطة الأشعة الكونية وانشطارات نووية، ولكن هذه الكمية من هذا النظير لا تتوفر إلا من خلال انفجار نجم. مع أن عمر النصف للنظير يود-129 قصير نسبيا بالمقارنة مع الفترات الزمنية للكون، عمر النصف لهذا النظير يبلغ 16 مليون سنة فقط، هذا يثبت أنه لم يمر إلا وقت قصير بين انفجار النجم وبين تجمد النيزك واحتجازه للنظير يود-129، هذين السببين (انفجار النجم وتجمد سحابة الغازات) يدلان على حدوث هذا في التاريخ المبكر للنظام الشمسي، وأيضا النظير يود-129 من المحتمل تكونه قبل تكون النظام الشمسي، ولكن ليس قبله بفترة طويلة، وقام ببذر أيونات سحابة الغازات الشمسية مع نظائر من مصدر آخر، ربما يكون انفجار النجم سببا لانهيار سحابة الغازات الشمسية. كان الاعتقاد السائد لفترة طويلة بأن الزينون والغازات النبيلة الأخرى خاملة كيميائيا وليست قادرة على الدخول في مركبات، على الرغم من ذلك، اكتشف نيل بارتليت خلال تدريسه في جامعة كولومبيا البريطانية أن غاز سداسي فلوريد البلاتين (PtF6) هو عامل أكسدة قوي يستطيع تحويل غاز الأكسجين (O2) إلى ثاني أكسيد سداسي فلوريد البلاتين [O2[PtF6، وبما أن جهد التأين الأول لكل من الأكسجين والزينون متقارب، أدرك بارتليت أن سداسي فلوريد البلاتين ربما يكون قادرا على إجراء تفاعل مع الزينون. في 23 مارس 1962، قام بارتليت بخلط الغازين معا وأنتج أول مركب كيميائي معروف لغاز نبيل: سداسي فلوريد بلاتين الزينون، اعتقد بارتليت خلال عملية التحظير هذا المركب أنه من الممكن وجود العديد من أملاح الزينون. منذ ذلك الحين، تم اكتشاف العديد من مركبات الزينون وتم التعرف على مركبات لغازات الكريبتون والرادون والأرجون مثل هيدرو فلوريد الآرجون (HArF) وثاني فلوريد الكريبتون (KrF2) وفلوريد الرادون (RnF).
الخصائص
[عدل]
وميض / بريق زينون: ذرة زينون هي معرفة بأنها تحتوي على نواة بـ54 بروتون تحت درجة حرارة وضغط قياسيين، غاز زينون النقي له كثافة ك 5.761 كغ/ م3 حوالي 45 مرات الكثافة السطحية لجو الأرض 1.217 كغ/ م3 كسائل >.[7] «زينون» له كثافة تساوي أو تفوق 3.100 غ/ل مع كثافة قصوى تحدث عند النقطة الثلاثية. تحت نفس الظروف كثافة زينون وهو صلب تعادل 3.640غ/ سم3وهي أعلى من كثافة المتوسطة للغرانيت 2.75 غ/ سم3 باستعمال giga pascal للضغط يتم اقحام «زينون» في مرحلة المعادن phase يتحول عنصر «زينون» الصلب من تكعيب وجه مركز ((hcp) (fcc هيكساغونال باكت وهي مرحلة كريستالية تحت الضغط تبدأ بالتحول إلى معدنية في حوالي 140 gpa دون ملاحظة تغير في الحجم في مرحلة hcp. هي معدن بالكامل 155 gpa. عند التمعدن عنصر «زينون» يبدو أزرقا سماويا لأنه يمتص الضوء الأحمر ويحول ترددات مركبة أخرى. هذا السلوك غير عادي بالنسبة لمعدن ويمكن شرحه بقصر سمك الروابط الإلكترونية نسبيا في عنصر زينون المعدني. «زينون» هو عضو من العناصر ذات valence الخارجية تحتوي على ثمانية إلكترونات. هذا ينتج رسم بيان أدنى وثابت للطاقة الذي من خلاله الإلكترونات الخارجية مرتبطة بإحكام. إلا أن عنصر «زينون» يمكن أن يؤكسد بعوامل أو عناصر مؤكسدة قوية وعدة مركبات كزينونية تم تركيبها. في أنبوب مليء بالغاز كزينون يبعث بريقا أو خزامى عندما يثار الغاز بإفراغ كهربائي يبعث أو يخرج كزينون مجموعة من أسطر أو خطوط الانبعاث التي تقرن الطيف المرئي إلا أن أغلب الخطوط الشديدة تظهر أو تحدث في منطقة اللون الأزرق الذي ينتج التلوين.
المواصفات الفيزيائية
[عدل]ينتج الزينون المعدني بتسليط ضغط بعِدّة مئات كيلو بار. والزينون غاز نبيل أَو غاز خامل يوجد بكميات قليلة في الجوّ وبنسبة (أقل مِنْ 1 جزء بالمليون حجما)، كما يوجد في جو المريخ بحدود حوالي 0.08 جزء بالمليون. من صفات الزينون أنه عديم الرائحةُ وعديم اللون.
قبل عام 1962 اعتقد بأنّ غاز الزينون وبقية الغازات النبيلة الأخرى لا يمكن تَشكيل المركّبات منها. ومركّبات الزينون المعروفة الآن هي (الهيدرات، فوق زينتات الصوديوم، ديوتيرات، ثنائي الفلوريد، رباعي الفلوريد، سداسي الفلوريد)، (XePtF6)،(XeRhF6) والمتفجر العالي الانفجار المعروف بـ (ثلاثي أكسيد الزينون، XeO3).
يعطي أنبوب الزينون المفرغ من الهواء وهج أزرق عندما يهيج بالتفريغ الكهربائيِ ويستعمل في المصابيح ذات الضوء القوي الوهاج Strobe Lamp.
الزينون يحصل عليه كناتج عرضي مِنْ تسيل وتجزيئه الهواء تحت ضغط عالي. وهذا لا يُجرى عادة في المختبرات، والزينون متوفرُ بشكل تجاري ويجهز في أسطوانات ذات ضغط عاليِ.
الوقوع والإنتاج
[عدل]كزينون هو غاز أثر في جو الأرض إحداث أو تقع عند 1+-87 جزء من المليار أو تقريبا جزء من 11.5 مليون جزء ويوجد أيضا في الغازات المنبعثة من بعض الينابيع المعدنية. كزينون يتحصل عليه تجاريا كإنتاج مزدوج من تقسيم الهواء إلى أكسجين ونيتروجين بعد هذا الانقسام عادة ينجز بالتقطير الجزئي في نبات ذو عمودين الأكسجين السائل المحصل عليه سيحتوي على كميات قليلة من الكريبتون والكزينون. بواسطة خطوات إضافية للتقطير الجزئي. الأكسجين السائل يمكن تغذيته للحصول 0.1-02٪من مزيج الكريبتون والكزينون الذي يستخلص إما عن طريق الامتصاص على silicagel أو بالتقطير أخير. مزيج الكريبتون والكزينون يمكنه عزله إلى الكريبتون والكزينون عبر التقطير استخلاص لتر واحد من الكزينون من الجو يستلزم 220 سا/واط. الإنتاج العالمي للكزينون في 1998 قدر ب 5000-7000م3 بسبب نقص وفرته. كزينون أغلى من الغازات النبيلة الأخف وزنا الأثمان التقريبية لشراء كميات قليلة في أوروبا 1999 10 اورو بالنسبة لعنصر الكزينون و 1 أوروا /ل للكريبتون و 0.20 اورو/ل للنيون. داخل النظام الشمسي جزء النوى للكزينون هو 1.56x 10-8 لتوفير جزء في 64 من الكتلة الكلية. كزينون نادر رئيسيا في جو الشمس على الأرض وفي المذنبات والنيازك لكوكب المشتري وفرة عالية غير عادية من عنصر الكزينون في جزه حوالي 206 مرات أكثر من التي حول الشمس. هذه الوفرة العالية تبقي غير مفهومة وتكون غالبا نتيجة بناء قديم وسريع للكويكبات قبل اشتعال presolar disk مشكل الكيزون الأرضي المنخفض يمكن شرحه covalent bonding من كزينون إلى أوكسجين داخل quartz مما يؤدي إلى انخفاض الغاز الكزينون المنبعث إلى هواء. عكس الغازات النبيلة ذات الكتل القليلة العملية العادية ل stellar نيكليو سينتاسيس داخل نجم لا تشكل كزينون عناصر أكثر كتلة من الحديد irom56 عندها مقدار الطاقة صافي الإنتاج عبر الذوبان. إذن ليس هناك ربح للطاقة لنجم عند إنتاج كزنون عوضا من ذلك يشكل كزينزن خلال انفجارات بواسطة عملية الحصول على النيترون sprocess للنجوم الحمراء العملاقة التي تبعث الهيدروجين إلى بواطنها وتدخل asymptoptic giand branch الجدر العملاق الاسيمتوبتيكي في الانفجارات الكلاسيكية novae وتشكل تآكلا إشعاعيا لعناصر مثل الايودين واليورانيم والبلوتو نيم.
النظائر المشعة ودراسات النظائر (الاسوتوبات والدراسات الاسوتوبية)
[عدل]وجود كزينزن طبيعيا مكون من تسعة نظائر ثابتة جامدة الأكثر من أي عنصر باستثناء tih الذي يتكون من عشرة كزينون و tim هما فقط العنصران الذي لهما أكثر من سبعة اسوتوبات ثابتة. اسوتوبات Xe124 ,Xe134، Xe136، يتنبا انهما تستطيع تحمل تآكل beta المزدوج لكن هذا لم يلحظ قط لهذا يعدون عناصر ثابتة إضافة إلى هذه الأشكال الثابتة هناك أكثر من 40 اسو توب غير ثابة تتم دراستها. ينتج بتآكل beta I129 الذي يملك نصف حياة 16 مليون سنة في حين أنXe131M 135 Xe133M ,Xe134 ، Xe133 هب بعض من منتجات FISSION لكل من U235 و Pu39 واذن تستعمل كدلائل أو مشيرات للانفجارات النووية. نويات اثنين من النظائر والكزينون الثابتة X2 129 و X2 131 لها non zero intrissic anguler montent. الدورات النووية يمكن ترتيبها ما وراء مستويات الاستقطاب العادية بواسطة ضوء الاستقطاب الدائري وبخار rudbiridium الاستقطاب الدائري الناتج عن نويات الكزينون يمكن أن تفوق 50 من قيمتها القصوى الممكنة. سابقة القيمة القصوى لدرجة حرارة غرفة، حتى في أقوى المغانط. هذا الترتيب الغير متوازن للدورات هو ظرف أني ويسمى hyperpolarisation هذه العملية للكزينون تسمى opticapunping رغم أن هذه العملية مختلفة عن ضخ أشعة الليزر. لان نوى 139 Xeله دوران1/2 وعليه zéro Electric quadra pole moment لحظة صفر الكهرباء، نوى 139 Xe لا يختبر أي تفاعل quadra pole خلال التصادم مع ذرات أخرى. ولهذا hyperpolarisation خاصته يمكن السيطرة عليه لفترات طويلة من الوقت حتى بعد إطفاء شعاع الليزر وإخلاء أو تفريغ بخار alkaliبالتكثيف على مساحة درجة حرارة الغرفة. الدوران الاستقطاب 139 Xeيمكنه الصمود لبضعة ثوان بالنسبة لذرات الكزينون المنحلة في الدم لبضع ساعات في مرحلة الغاز ولعدة أيام في الكزينون الصلب الشديد البرودة. على العكس 131 Xeله قيمة دوران نووي تعادل 2/3 zéro Electric quadra pole moment كما له 5 مرات من التراخي في سلم الميلثانية (ms) وسلم الثانية (s). بعض الاسوبات الإشعاعية للكزينون مثل 133 Xe و135 Xeتنتج بالنيوترون عديم الإشعاع لمعدن fission able داخل المفاعلات النووية 135 Xeذو أهمية معتبرة في عملية مفاعلات fission النووية. 135 Xe له قطاع cross هائل للنيوترنات الحرارية 6 x 102.6 بارن. لذا يعمل لماص للنيوترتنات أو يمكنه إبطاء أوقف التفاعل التسلسلي بعد مدة من العملية. اكتشف هذا في المفاعلات النووية الأولى المركبة من طرف مشروع ماتلتن الأمريكي لإنتاج البلوتنيوم. لحسن الحظ المصممون اوجدوا ذخائر ومستلزمات في التصميم لزيادة رد فعل المفاعل (عدد النيوترونات في fission التي تتابع fission ذرات أخرى لوقود نووي).تسمم مفاعل 135 Xeلعب دورا هاما في حادثة تسنوبل. توقيف وانخفلظ طاقة مفاعل يمكن أن ينتج عنها تكوين 135 Xe والحصول على المفاعل في iodine pit. تحت ظروف معاكسة أو مضادة نسبيا التركيزات العالية لاسوتوبان الكزينون الاشعاعية يمكن إيجاده منبعثة من المفاعلات النووية بسبب إطلاق منتجات fission من تصدع قضبان الوقود أو fissioning اليورانيوم في الماء البارد. لأن كزينون راسم اثر لاثنين من الاسوتوبات معدلات السوتوب الكزينون في النيازك تعتبر وسيلة قوية لدراسة تكوين النظام الشمسي. طريقة كزينون الايدونيني للتاريخ تعطي الوقت المنقضي بين النظرية النووية وكثافة الشيء الصلب من nebulla الشمسي في 1960 الفيزيائي جون رينولدز اكتشف ان بعض النيازك تحتوي على شذوذ اسوتوبي على شكل وفرة عارمة من 129 xeron استنتج ان هذا كان تاكل الناتج من إشعاع ايودين 129 هذا الاسوتوب ناتج ببطا بواسطة fission cosmic ray spallation النووي. ولكن ناتج بكمية فقط بانفجارات supermorda اما بالنسبة لنصف حياة 129I هو قصير بالمقارنة على السلم الزمني الكوني فقط 16 ملون سنة اظهر بين هذا ان زمنا قصيرا فقط معنى SUPERNOVA ووقت تصلب النيازك واحتباس 129I. هذان الحدثان تم استنتاجهما على إنهما حدث خلال العهد أو التاريخ القديم للنظام الشمسي. فيما يخص اوستوب 129I انتج تكوين النظام الشمسي لكن ليس بوقت بعيد. وزرع كتلة الغاز الشمسي باوستوبات من مصدر SUPERNOVA هذا قد يكون سبب انهيار أو دمار سحابة الغاز الشمسي. بطريقة مماثلة درجات كزينون الاسوتوبي Xe130 Xe136 Xe130 Xe129هما أيضا وسيلة جد قوية وهامة لفهم الاختلاف الكويكبي والانبعاث الخارجي للغاز في القديم مثل الجو أو هواء المريخ يظهر ان وفرة كزينون شبيهة بالتي على الأرض 0..8/جزء مليون. لكن المريخ يظهر نسبة 129 Xeاعلي من التي على الأرض أو على الشمس. بما أن هذا الاسوتوب ينتج عن تآكل إشعاعي النتيجة يمكن أن تشير إلى أن المريخ فقد أغلب هوائه prinordial ربما خلال المائة مليون سنة الأولى بعد تكون الكوكب. في مثال آخر شدة Xe129 الموجودة في ثاني اوكسيد الكربون الخاص بالغازات المخزنة في نيومكسيكو أعتقد أنها من تآكل الغازات المشتقة من mantle قريبا من تشكل الأرض.
مركبات الزينون
[عدل]بعد أن اكتشف نيل بارتلت الإكزنون Xenon يمكن أن يشكل تركيبة كيميائية، هناك عدد كبير من أنواع الإكزنون Xenon المركب تم اكتشافه ووصفه. من المعلوم أن تركيبة الإكزنون Xenon تحتوي على جزيئات الفليورين الإلكتروسالبة أو جزيئات الأكسجين. هناك ثلاث أنواع من الفلوريد مثل ثنائي فلوريد الزينون XeF2، ورباعي فلوريد الزينون XeF4، وسداسي فلوريد الزينون XeF6. الفلوريد هو نقطة بداية لبناء كل تراكيب الإكزنون Xenon، ويشكل الفليوريد البلوري الصلب XeF4، عند امتزاج غاز الفليورين المعرض للأشعة مافوق البنفسجية، أي التعرض لضوء نهار يومي كاف لإتمام هذه العملية. -يسخن XeF4 على درجة حرارة عالية بمساعدة وسائط كيميائية من XeF6 في حضور NAF. يلعب الإكزنون Xenon دور المستقبل حاله حال مستقبلات الفليوريد ومرسلات الفليوريد، بتشكيل الأملاح التي تحتوي على أيونات الموجبة مثل XeF+، XeF3 والشوارد مثل XeF5، XeF7، XeF8. يتشكل Xe+2 في المجال المغناطيسي القريب من اللون الأخضر، من نقص جزيئة XeF2 وغاز الإكزنون Xenon، ويمكن XeF2 أن يتشكل أيضا من ترابط المركبات مع أيونات المعادن المتحولة، أكثر من 30 نوع من المركبات تم بنائها وتخصيصها. كما أن فليوريدات الإكزنون Xenonمصنفة بطريقة جيدة في حين، أن Halides غير معروفة والإنشاء الوحيد هو الديكلوريد XeCl2، يجهز الإكزنون Xenon الديكلوريد ليصبح تركيبة بلورية غير ملونة لها حرارة داخلية والتي تتفكك في درجة حرارة 80C°من ترددات الإشعاعية العالية الناتجة عن امتزاج الإكزنون Xenon، الفليورين، السيليكونو الكاربون. وهناك احتمال أن تتراكلوريد Tetra-cloride يرتفع تحت تأثير الطقس، أي أن هناك علاقة طردية. XeCl هو تركيبة حقيقية وليس جزيئات الفندروالس Vanderwaals متكونة من مجموعات Xe الضعيفة وجزيئات Cl2 وقد أشارت بعض الحسابات النظرية أن الجزيئات الخطية XeCl2 هي أقل ثبات من مركب الفندروالس Vanderwaals.
الأكسيد والأكسوهاليد
[عدل]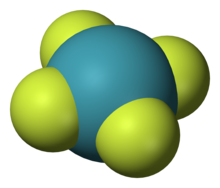

هناك ثلاث أكسيدات من الكزينون معروفة هي ثلاثي أكسيد الزينون Xe O3 و (رباعي) تترو أكسيد الكزينون Xe O4 كلاهما عناصر خطيرة متفجرة وقوية ومؤكسدة. ثاني أكسيد الكزينون Xe O2 روج وأشيع سنة 2011 مع رقم مساواة من4، Xe O2 يتكون عندما يصب فليوريد الكزينون على الجليد. بنيته البلورية كريستالية قد تسمح له باستبدال السلوكون في المعادن والأملاح السليكاتية SILICATE. XeOO+ شاردة موجبة تم تعريفها عن طريق أشعة INJRATRED SPEDRSAPY في جزيئة الأرغون الصلبة. في المصابيح لا يتفاعل كزينون مع الأكسجين مباشرة، ثلاثي الأكسيد يتشكل بواسطة hudrolysis التحلل المائي ل Xe F6 وفق المعادلة التالية: Xe F6 + 3 H2o ---- XE O3 + 6HF XE O3 هومركب ضعيف حامضيا متحلل في ALKALLI لتكوين تشكيل أملاح xenate غير ثابتة (مستقرة) تحتوي على XeO-4 anion H هذه الأملاح الغير مستقرة سهلة التناسب disproportion إلى كزينون وأملاح perscesnate محتوية على anion 6Xe O+ Perscente الباريوم عند معالجتها بحامض الكبريت المركز ينتج رباعي tetr BaXeO6+ 2H2SO4 → 2BaSO4 + 2H2o + XeO4 لمنع التحلل تاتروكسيد المتشكليبرد بسرعة لتشكيل نوع من الصلب الأصفر الشاحب ينفجر فوق 53.9 - درجة مئوية إلى كزينون وغاز الأكسجين عدد من أوكسيلفليوريدات الكزينون معروفة بما في ذلك XeOF2,XeOf4,XeO2F2,XeO3F2 XeOF2 يتكون بتفاعل OF2 مع غاز الكزينون في درجات حرارة منخفضة. يمك الحصول عليه أيضا بواسطة hydrolysis النسبي لـXeF4. يتجزأ (doproportiontes) في 20- درجة م إلى XeF2 وXeOF4. XeOf4 يتكون بالـ hydrolysis النسبي (الجزئي) لـ XeF6 أو يتفاعل XeF6 مع perscente الصوديوم Na4XeO6 تفاعل هذا الأخير ينتج أيضا كمية قليلة من XeO2F2. XeOF4 ِ يتفاعل مع CsF لتكوين XeOF-5 anion في حين يتفاعل XeOF3 مع فليوريدات معدن RbF, kF alkali وِCs لتشكيل XeOF-4 anion بالإضافة إلى مركبات حيث يشكل زينون ترابط الكيميائي، ويمكن للزينون تشكيل في الشكل، حيث تكون ذرات الزينون محاصرة من قبل شعرية البلورية من مركب آخر. ومن الأمثلة على هيدرات زينون (H2O اكس • 5,75)، حيث تشغل ذرات الزينون الفراغات في شعرية من جزيئات الماء. ولهذا المشبك نقطة ذوبان 24 درجة مئوية.و قد تم إنتاج إصدار بالديوتيريوم من هذا هيدرات ومشبك هيدرات هذا يمكن أن يحدث بشكل طبيعي في ظل ظروف الضغط العالي، كما هو الحال في بحيرة فوستوك تحت الغطاء الجليدي في القطب الجنوبي، ويمكن استخدام تشكيل مشبك لالأرجون، ومصابيح تقطير يمكن أيضا للزينون أن يشكل المركبات الفوليرين endohedral، حيث تحبس ذرة زينون داخل جزيء الفوليرين. ويمكن رصد ذرة زينون المحاصرة في الفوليرين 129Xe النووية عبر الرنين المغناطيسي الطيفي (الرنين المغناطيسي). باستخدام هذه التقنية، يمكن تحليل التفاعلات الكيميائية على جزيء الفوليرين، ونظرا لحساسية هذا التحول الكيميائي للذرة زينون مع بيئته. ومع ذلك، فإن ذرة زينون لها أيضا تأثير الإلكترونية على التفاعل الفوليرين. حينما تكون ذرات الزينون في حالة الطاقة الأساسية، فإنها تتنافر من بعضها البعض، وسوف لا تشكل صلة. عندما يتم تنشيط ذرات زينون، فإنها يمكن أن تشكل excimer (ديمر متحمس) حتى عودة الإلكترونات إلى الحالة الأساسية. ويتكون هذا الكيان لأن ذرة زينون تميل لملئ غلافها الإلكتروني الأبعد ويمكن باختصار القيام بذلك عن طريق إضافة الإلكترون من ذرة زينون المجاورة. العمر النموذجي لـلزينون excimerهو 1-5ms، وضمورها يطلق فوتونات بطول موجة من حوالي 150 نانومتر و173ناتومتر يمكن أيضا للزينون dimersأن يشكل مع العناصر الأخرى، مثل الكلور، الهالوجينات، والبروم، الفلور.
مركبات أخرى
[عدل]•مؤخرا كان هناك اهتمام بمركبات الكزينون أين يكون الكزينون مرتبط مباشرة بعنصر كهروسلبي (سلبي الكترون) أقل من الفليورين أو الأكسجين خاصة الكربون carbon. مجموعات انسحاب الإلكترون كمجموعات ببديل الفليورين، هامة (مهمة) لاستقرار هذه المركبات (العناصر المركبة). عدد من هذه امركبات تم تخصيصها (تميزها) بما في ذلك ِ-C-CH3≡C6F5-Xe+-N أين يكون C6F5 هو مجموعة النيتافليوروفينيل 2Xe[C6F5 ] C6F5-Xe-X أين X هو Cl، F، CN R-C≡C-Xe+ حيث R هو C2F-5 أو tertbutyl C6F5-XeF+ (C6F5Xe)2l+ •مركبات أخرى محتوية على كزينون مرتبط بعنصر كهروسلبي أقل يستلزم F-Xe-N(SO2F)2 و F-Xe-BF2. هذا الأخير مستخلص من تيترا فليوروبورات الديوكسيجينيل dioxygenyl O2BF4 في 100- درجة مئوية. •إيرن غريب (غير عادي) يحتوي على الكزينون هو شاردة تيتراكزينونوغراد (II) AuXe2+u الذي يحتوي على الروابط Xe-Au. هذا الأيون يحدث في المركب AuXe4(Sb2F11)2 وهو ملاحظ على احتوائه روابط كميائية مباشرة بين ذرتين غير متفاعلتين معروفتين ـ الكزينون والذهب مع الكزينون يعمل كرابط معدني انتقالي. •1995 السيد رازانان ومساعديه علماء في جامعة هيلسنكي في فنلندا أعلنوا عن تحضير ديهيدريد الكزينون HXeH ولاحقا هيدروكسيد-هيدريدالكزيون HXeOh، هيدروكزينوأسيتيلين HXeCCH وجزيئات أخرى تتحتوي على Xe. في 2008 خريشتشلف أعلن عن تحضير HXeOXeH بالـ phototolysis الخاص بالماء داخل مزيج الكزيون الكربوجيني (cryogenic). جزيئات HXeOD، Deuterted و DXeOH تم أيضا إنتاجهما.
الاستخدامات
[عدل]يستخدم الزينون في ملء زجاجات المصابيح الكهربائية ذات الاستخدام الخاص وهو ذو كفاءة عالية. حيث تعطي مصابيح الزينون إضاءة قوية تقارب في سطوعها ضوء الشمس وتتميز بإضاءتها عن مصباح التنجستن هالوجين بثلاثة أضعاف مع توفير 40% بالطاقة الكهربائية المستهلكة فمصباح الزينون يحتوي على كبسولة زجاجية مضغوط بها غاز الزينون مع خليط من غازات أخرى قابلة للاشتعال ويحتاج خليط الغازات داخل مصباح الزينون إلى نظام كهربائي خاص يوفر فولتية عالية تصل إلى 25 كيلو فولت لتشغيل المصباح. ومن استخدامات الزينون أيضا في يومنا هذا انه أصبح يستخدم في اضواء السيارات الحديثة، فتوضع لمبة الزينون في مصباح السيارة فتعطي قوة ضوء أقوى بثلاث مرات من الهالوجين العادي (الضوء الأصفر) لذلك أصبح الزينون من الأشياء الضرورية في الحياة. هو فلاش حقيقي وليس ضوء عادي يستخدم في المناطق المعتمة جداً وهو يعطي إنارة قد اتصل لعشرات الأمتار وقادر على إنارة أكثر من 30 متراً إنارة كاملة ويعطي سطوع يماثل سطوع ضوء الشمس في قوته أو ثلاثة أضعاف الإضاءة العادية بالتنجستن هالوجين مع توفير طاقة تقدر بـ 40% وعمر تشغيلي أكبر. يستخدم الإكزنون لصناعة فلاش الإكزنون ومصابيح الإكزنون خاصة في السيارات الزينون الذي يتفاعل كيميائياً وعند هذا التفاعل يطلق نوراً شديداً لأجزاء من الثانية. - يحتاج الهاتف أو الكاميرا المزودة بغاز الإكزنون Xenon أن تعيد شحن الغاز مرة أخرى كي يستعد لإطلاق الصورة الثانية وهي تستغرق في بعض الحالات أجزاء من الثانية. فلاش الإكزنون Xenonالموجود في الكاميرات نلاحظ أنه يحتوي على كبسولة زجاجية موجود فيها غاز الإكزنون Xenonمع خليط من غازات أخرى قابلة للاشتعال في حالة توفر طاقة كهربائية قادرة على التفاعل مع هذه الغازات وهي 25 كيلو فولت وهو الأمر الذي يجعل الفلاش يستهلك طاقة الهاتف بشكل أكبر. يستخدم ضوء الإكزنون Xenon في السيارات الحديثة أيضاً بحيث نلاحظ الفرق بين ضوء سيارة (الأبيض القوي) و (الأبيض المائل للصفرة) الأقل نوراً منها.
تطبيقات
[عدل]على الرغم من أن الزينون نادر وباهظ الثمن نسبيا لاستخراج من الغلاف الجوي للأرض إلا أن له عدد من التطبيقات.
الإضاءة والبصريات
[عدل]مصابيح تفريغ الغاز
[عدل]يستخدم الزينون في أجهزة التي تشع ضوءا تدعى مصابيح فلاش زينون، والتي تستخدم في التصوير الضوئي ومصابيح اصطرابي؛ لإثارة المتوسطة الناشطة في الليزر التي تولد ضوء متماسك؛ وأحيانا في المصابيح جراثيم. اخترع ليزر الحالة الصلبة الأولى، في عام 1960، تم ضخها من قبل مصباح زينون فلاش، وأشعة الليزر المستخدمة في الانصهار الحبس بالقصور الذاتي من جانب مصابيح زينون فلاش.


لمصابيح الزينون المستمرة ذ ات الضغط العال درجة حرارة اللون تقارب وثيق ضوء الشمس ظهرا ويتم استخدامها في أجهزة محاكاة الشمسية. أي أن اللونية لهذه المصابيح تقترب كثيرا من مشعاع ساخنة الجسم الأسود الذي يحتوي على درجة حرارة قريبة لتلك الملاحظة من الشمس بعد أن تم تقد مها لأول مرة خلال الأربعينيات (1940s)، بدت هذه المصابيح بديلة لمصابيح الكربون قصيرة القوس (الأقصر عمرا) في شاشات السينما. تستخدم في 35mm نموذجية ونظم آيماكس الإسقاط في الفيلم، لمبات المصابيح الأمامية للسيارات، بالإضافة إلى استخدامات متخصصة أخرى. يعد قوس هذه المصابيح مصدر ممتاز من الأشعة فوق البنفسجية قصيرة الموجة ولديها انبعاثات مكثفة في الأشعة تحت الحمراء القريبة، والذي يستخدم في بعض نظم الرؤية الليلية. تستخدم الخلايا الفردية في عرض البلازما خليط من مصابيح النيون وزينون التي يتم تحويلها إلى البلازما باستخدام الأقطاب الكهربائية. تفاعل البلازما مع هذه الأقطاب الكهربائية تولد فوتونات الأشعة فوق البنفسجية، والتي تثير ثم طلاء الفوسفور الذي يغطي واجهة العرض. يتم استخدام الزينون بأنه «كبداية الغاز» في مصابيح الصوديوم ذات الضغط العالي، لديها أدنى موصلية حرارية وأقل جهد التأين من جميع الغازات النبيلة غير المشعة. كغاز الزينون، فإنه لا يتداخل مع التفاعلات الكيميائية التي تحدث في مصباح التشغيل. والموصلية الحرارية المنخفضة تقلل من الخسائر الحرارية في المصباح في حين أنه في حالة التشغيل، وجهد التأين المنخفضة يحسب انهيار جهد الغاز لتكون منخفضة نسبيا في الحالة الباردة، والذي يسمح للمصباح أن يكون أكثر سهولة لبدء التشغيل. الزينون هو أكبر وأثقل الغازات النبيلة غير المشعة وذلك معدل الانتشار والتسرب من خلال الزجاج أو أغلفة أخرى ضئيل بالنسبة إلى الغازات الخاملة البديلة. عند 169م/ ث، سرعة الصوت في غاز الزينون أبطأ من ذلك في المواد وهذا راجع إلى السرعة المتوسطة الأبطأ لذرات الزينون الثقيلة مقارنة مع جزيئات النيتروجين والأكسجين، وبالتالي، زينون يقلل من ترددات الرنين من الجهاز الصوتي عند استنشاقه. ونتج هذا صوتا منخفضا متميزا، تأثير معاكس لصوت عال timbred الناجم عن استنشاق الهيليوم مثل الهليوم، زينون لا يلي حاجة الجسم للأكسجين. زينون على حد سواء خانق بسيطة ومخدر أقوى من أكسيد النيتروز، وبالتالي لم يعد العديد من الجامعات تسمح لحيلة الصوت لعرض الكيمياء العامة. بما أن زينون مكلف (غال) فإن سادس فلوريد الكبريت الغاز، وهو ما يماثل زينون في الوزن الجزئي (146 مقابل 131)، وتستخدم عموما في هذه الحيلة، ويعتبر خانق من دون أن يكون مخذّرا. من الممكن أن تتنفس بأمان الغازات الثقيلة مثل زينون أو سادس فلوريد الكبريت عندما يكونون في خليط مع الأكسجين، والأكسجين التي تضم ما لا يقل عن 20 % أكسجين ينتج بسرعة غيبوبة التخدير العام (واستخدمت لهذا، كما نوقش أعلاه). الاستنشاق يمزج غازات من كثافات مختلفة على نحو فعال وسريع جدا بحيث يتم إزالة الغازات الثقيلة مع الأكسجين، ولا تتراكم في الجزء السفلي من الرئتين وهناك مع ذلك، فإن خطر مرتبط مع أي غاز ثقيل بكميات كبيرى: فهو يقبع بخفاء في وعاء، وإذا دخل أي شخص إلى حاوية مليئة الغاز عديم اللون والرائحة، فإنه قد يجد نفسه يتنفسه دون دراي، ونادرا ما يستخدم زينون بكميات كبيرة بما يدعو لهذا القلق، على الرغم من احتمال وجود خطر في أي وقت بخزان أو حاوية من الكزيون يتم الاحتفاظ بها في مساحة عديمة التهوية. وزينون يعمل أفضل 5 neuroprotectant من الكيتامين أو أكسيد النيتروز، والتي لها آثار جانبية غير مرغوب فيها ثم إضافة غاز الكنزينون باعتباعره عنصرا من مزيج التهوية لمولود الجديد في سانت مايكل، بريستول، انكلترا، والذين تعرضت فرص فرص حياتهم للخطر لأنه ناجح، مما أدى لإلى إذن من التجارب السريرية لحالات مماثلة.
ليزر
[عدل]قام في 1962، مجموعة من الباحثين في مختبرات بيل باكتشاف عمل الليزر في زينون، ووجدوا لاحقا أنه تم تحسين الحصول على ليزر الهليوم عن طريق إضافة إلى إصدار إشعاعات منتظمة مثل الليزر المتوسطة. ليزرالإكرايمز (excimer) أول استخدام ديمر زينون (Xe2) لتنشيطه بواسطة شعاع من الإلكترونات لإنتاج حفز الانبعاثات في الطول الموجي والأشعة فوق البنفسجية من 176 نانومتر. كلوريد زينون فلوريد الزينون المستخدمة في الليزرexcimer (أو، بدقة أكبر، الليزر exciplex). استخدم زينون الفلوريد والزينون الكلوريد في الليزر excimer، على سبيل المثال، في بعض الأمراض الجلدية.
طبية
[عدل]التخدير
[عدل]وقد استخدم الزينون كمخدر عام. على الرغم من أنه مكلف، وآلات التخدير التي يمكن أن تنقل زينون على وشك أن تظهر في السوق الأوروبية، وذلك لأن التقدم في الانتعاش وإعادة تدوير الزينون من هذه الآلات ناجحة اقتصاديا. وقد اقترحت آليتان الفسيولوجية للتخدير زينون. أولها ينطوي على تثبيت آليات مضخة الكالسيوم أتبازatbase) (اتي تستخدمها الخلايا لإزالة الكالسيوم (Ca2 +) في غشاء الخلية من نقاط الاشتباك العصبي. وهذا ناتج عن تغيير متعلق بتكوين جزئي عندما يربط زينون إلى مواقع الغير قطبية داخل البروتين. أما الآلية الثانية تركز على التفاعلات غير محددة بين مخدر والغشاء الدهني. للزينون الحد الأدنى من تركيز السنخية (ماك) من 72 ٪ في سن ال 40، مما يجعل 44 ٪ أكثر فعالية من أكسيد النيتروز (N2O كمخدر. وهكذا يمكن استخدامه في تركيزات مع الأكسجين الذي يقل لديهم خطر نقص الأكسجة. وخلافا أكسيد النيتروز (N2O) زينون ليس غازات الدفيئة وذلك يعتبر أيضا أنها صديقة للبيئة. للزينون تنفيس في الجو ويجري عاد إلى مصدره الأصلي، لذلك لا الأثر البيئي المحتمل. للزينون حامي عصبي في علاج إصابات المخ والجروح الدماغية، لأنه خصم لمستقبلات ن ميثيل مد اسبارتاتي (مستقبلات NMDA). هذه المستقبلات تفاقم الضرر الناجم عن الحرمان من الاكسجين فيعمل الزينون كحامي عصبي أفضل من الكيتامين أو أكسيد النيتروز، والتي لها الآثار الجانبية. تمت إضافة غاز الزينون باعتباره عنصرا من مزيج التهوية عند المولود الجديد في مستشفى سانت مايكل، ببريستول، انكلترا، والذين أصبحت فرص حياتهم واعدة وناجحة، مما أدى إلى السماح باستعماله في التجارب السريرية لحالات مماثلة.
التصوير
[عدل]ويمكن استخدام انبعاثات غاما من Xe133 النظائرالمشعة من الزينون لتصوير القلب والرئتين، والدماغ على سبيل المثال، عن طريق الإشعاع الأحادي الفوتون المبرمج. كما تم استخدام Xe133 لقياس تدفق الدم. الزينون، ولا سيما العالي الاستقطاب Xe129، عامل تباين مفيد للتصوير بالرنين المغناطيسي. في المرحلة الغازية، ويمكن استخدامه لتصوير المساحات فارغة مثل صورة تجاويف في عينة المسامية أو الحويصلات الهوائية في الرئتين. وقد استخدمت فرط الاستقطاب يجعل 129Xe اكتشاف أكثر من ذلك بكثير عبر التصوير بالرنين المغناطيسي لدراسة والرئتين والأنسجة الأخرى. ويمكن استخدامه، على سبيل المثال، لتتبع تدفق الغازات داخل الرئتين. لأن زينون قابل للذوبان في الماء، وكذلك في المذيبات المائية، ويمكن استخدامه للحصول على صورالعديد من الأنسجة الحية الينة.[8]
رنين المغناطيسي النووي للزنون
[عدل]رنين المغناطيسي النووي Nuclear magnetic resonance أو اختصارا (إن.إم.آر NMR) هي إحدى الظواهر الفيزيائية التي تعتمد على الخواص المغناطيسية الميكانيكية الكمومية لنواة الذرّة. الرنين النووي المغناطيسي أيضا يستخدم للدلالة على مجموعة منهجيات وتقنيات علمية تستخدم هذه الظاهرة لدراسة الجزيئات من بنية وتشكيل فراغي. بسبب إتساع المسافة بين المدارات الخارجية في ذرة زينون واختلاف الظروف الكيميائية باختلاف الظروف البيئية المحيطة بها (ضوء، غازات..) يحدث تغير لطيف الرنين المغناطيسي النووي فعلى سبيل المثال عند ذوبان الزينون في الماء ثم إضافة بروتينات يمكن تمييز هذه البروتينات في المذيب بواسطة الرنين المغناطيسي كما يمكن أيضا استعمال مصابيح Hyperpolarized لوصف أسطح المواد باستعمال الرنين المغناطيسي النووي وذلك لأنه سيتم بعث إشارات من سطح العينة تتغير كتلة الأنوية الذرية وهذا ما يظهر في الاستقطاب بشكل انتقائي لغاز الزينون. وهذا يجعل من سطح إشارات قوية بما يكفي لقياس إشارات بكميات كبيرة.[9]
إستعمالات أخرى للزينون
[عدل]في تطبيقات الطاقة النووية، ويستخدم الزينون في غرف الفقاعات، من أجل التحقيقات، وغيرها من المجالات حيث الوزن الجزيئي عالي والطبيعة الخاملة غير مرغوب فيها. إحدى النتائج الجانبية لاختبار سلاح نووي هو إطلاق زينون133 - وزينون 135 المشعة -. يتم استخدام الكشف عن هذه النظائر لرصد الامتثال للمعاهدات حظر التجارب وكذلك تأكيد تفجيرات التجارب النووية من جانب الدول مثل كوريا الشمالية. يجري اختبار نموذج أولي لمحرك الزينون الأيوني في مختبر ناساللدفعjet.

يتم استخدام الزينون السائل في سعرات حرارية لقياس أشعة غاما، فضلا عن وسيط للكشف عن جسيمات افتراضية ضخمة ضعيفة التفاعل، أو wimp. عندما يصطدم wimp مع نواة زينون، فإنه ينبغي، نظريا قطاع الإلكترون وخلق التلألؤ الابتدائي. باستخدام الزينون، يتم تمييزهذه الطاقة المتولدة بسهولة من الأحداث المماثلة التي تسببها الجزيئات مثل الأشعة الكونية. ومع ذلك، فإن تجربة الإطلاق في مختبر غران ساسو الوطنية في إيطاليا وII ZEPLIN والتجارب ZEPLIN III في مختبر Boulby تحت الأرض BOULBY في المملكة المتحدة حتى الآن فشلت في العثور على أي تأكيد wimps. وحتى لو تم الكشف عن أية wimps، سوف تعمل التجارب على تقييد خصائص المادة المظلمة وبعض نماذج الفيزياء. والكاشف الحالي في مرفق غران ساسو أظهرت حساسية مماثلة لتلك التي استعملت للكشف عن أفضل مبردة، وكان من المتوقع أن تزيد الحساسية بأمر بالغ الأهمية من ضخامة في 2009. زينون هو الوقود المفضل لدفع الأيوني لمركبات الفضائية نظرا لقدرته التأين المنخفضة في الوزن الذري، وإمكانية تخزينه كسائل في درجة حرارة الغرفة الأدنى (تحت ضغط عال) بعد تحويله بسهولة مرة أخرى إلى غاز لتغذية المحرك. الطبيعة الخاملة من الزينون تجعله صديق للبيئة ومقلل لتآكل المحرك إلى الأيوني من أنواع الوقود الأخرى مثل الزئبق أو السيزيوم. استخدم لأول مرة الزينون لمحركات الأقمارالصناعية أيون خلال السعينيات 1970 استعمل في وقت لاحق بوصفه دافع لمركبات (سمارت SMRT.1 الفضائية في أوروبا وايون لمحركات الدفع ثلاثي على المركبات الفضائية التابعة للناساناسا. كيميائيا، تستخدم مع مركبات perxenate كما المواد المؤكسدة في الكيمياء التحليلية. يتم استخدام الزينون باعتبارها etchant للسيليكون، وخاصة في إنتاج أنظمة ميكانيكية إلكترونية صغيرة (mems) يمكن إنتاج الأدوية المضادة للسرطان (5 – فلورويوراسيل) من تفاعل الزينون مع الدفلوريد واليوراسيل يستخدم أيضا الزينون في البلورة البروتينية. بتطبيقه على الضغوط 0,5 حتي 5 ميغاباسكال (5-50 أجهزة الصراف الآلي) لبلورة البروتين، وترتبط ذرات الزينون في تجاويف هدروفوبية، وخالقتا في كثير من الأحيان مشتق الثقيل ذرة متجانس وذو الجودة العالية، تساوي الشكل، والتي يمكن أن تستخدم في حل مشكلة المرحلة.
الاحتياطات
[عدل]العديد من المركبات المحتوية على الأوكسجين الزينون تعتبر سامة وذلك بسبب خصائص قوة أكسدتها، ومتفجرة بسبب ميلها لكسر الروابط في الزينون بالإضافة إلى عنصري الأكسجين ثنائي الذرة (O2) والذي يحتوي على الروابط الكيميائية أقوى بكثير من مركبات الإطلاق. يمكن حفظ غاز الزينون بأمان في الزجاج العادي أو مختومة الحاويات المعدنية في درجة الحرارة والضغط المطلوبة ومع ذلك، فإنه يذوب بسهولة في معظم منتجات البلاستيك والمطاط، ويتسرب تدريجيا من حاوية مغلقة مع مثل هذه المواد. الزينون غير سام، على الرغم من أنه لا يذوب في الدم وينتمي إلى مجموعة مختارة من المواد التي تخترق جدار الدماغ الدموي، مما يسبب التخديرالخفيف للجراحة العامة عند استنشاقه في تركيزات عالية مع الأكسجين.[10] في 169 م / ث، سرعة الصوت في غاز الزينون أبطأ من ذلك في الهواء ونظرا لتباطئ سرعة ذرات الزينون الثقيلة مقارنة مع جزيئات النيتروجين والأوكسجين. وبالتالي، يقلل الزينون من ترددات الرنين من الجهاز الصوتي عند استنشاقه. وتنتج هذه سمة خفض صوت جرس، ولها تأثير معاكس للأصوت العالية الناجمة عن استنشاق الهيليوم. مثل الهليوم، زينون لا يلبي حاجة الجسم للأوكسجين. زينون على حد سواء خانق بسيط ومخدر أقوى من أكسيد النيتروز، وبالتالي لم يعد العديد من الجامعات تسمح للحيلة صوت كتعبير الكيمياء العامة. لأن الزينون باهظ الثمن، وتستخدم عموما غاز سادس فلوريد الكبريت، وهو ما يماثل زينون في الوزن الجزيئي (146 مقابل 131)، في هذه الحالة، ويعتبر خانقة من دون أن يكون مخدر. فمن الممكن أن تتنفس بأمان الغازات الثقيلة مثل زينون أو سادس فلوريد الكبريت عندما يكونان في خليط مع الأكسجين، والأوكسجين يضم ما لا يقل عن 20٪ من الخليط. الزينون تركيز 80٪ مع 20٪ أكسجين ينتج بسرعة غيبوبة التخدير العام (واستخدمت لهذا، كما نوقش أعلاه). استنشاق خليط غازات من كثافات مختلفة على نحو فعال وسريع جدا بحيث يتم إزالة الغازات الثقيلة مع الأكسجين، ولا تتراكم في الجزء السفلي من الرئتين، ومع ذلك، فإن الخطر المرتبط بأي غاز ثقيل بكميات كبيرة وارد: ربما............. في وعاء، وإذا دخل الشخص مكان مليئ بغاز عديم اللون والرائحة، فإنه إنه يستنشقه دون أن يدري. ونادرا ما يستخدم زينون بكميات كبيرة بما يكفي لهذا القلق، على الرغم من احتمال وجود خطر في أي وقت خزان أو حاوية من الزينون يتم الاحتفاظ بها في مساحة عديمة التهوية.[11]
فوائد الزينون
[عدل]- يعطي إنارة أقوى من إنارة الضوء العادي صمام ثنائي باعث للضوء ولوناً أفضل.
- يمكن تركيبة مع شاتر عالي السرعة وعندها نحصل على صورة متوقفة للأجسام السريعة.
- باستعمال مصابيح الزينون في السيارات يمكن تقليص الوفيات الناجمة عن حوادث المرور بما يساعد على تحسين الرؤية الليلية للسائقين وفي الوقت ذاته يحسن القدرة على التركيز. ونتيجة لذلك، فإن الضوء الأبيض المائل للزرقة للمصابيح الأمامية من Xenon يطيل مسافة التوقف بحوالي 30-50 مترا وفقا للحقيقة القائلة بأن المزيد من الضوء يسمح بالكشف عن المواقف الخطرة بشكل أسرع من نفس المسافة.
عيوب الزينون
[عدل]- سرعة استهلاك للبطارية مقارنة بضوء صمام ثنائي باعث للضوء العادي.
مراجع
[عدل]- ^ [1]
- ^ Lide، David R. (2004). "Section 4, Properties of the Elements and Inorganic Compounds; Melting, boiling, triple, and critical temperatures of the elements". CRC Handbook of Chemistry and Physics (ط. 85th edition). Boca Raton, Florida: CRC Press. ISBN:0849304857.
{{استشهاد بكتاب}}:|طبعة=يحتوي على نص زائد (مساعدة) - ^ Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ "2 Researchers Spell 'I.B.M.,' Atom by Atom". New York Times نسخة محفوظة 25 فبراير 2018 على موقع واي باك مشين.
- ^ Eremets, Mikhail I. ؛ Gregoryanz, Eugene A.؛ Struzhkin, Victor V.؛ Mao, Ho-Kwang؛ Hemley, Russell J.؛ Mulders, Norbert؛ Zimmerman, Neil M. (2000). "Electrical Conductivity of Xenon at Megabar Pressures". فيزيكال ريفيو Letters. ج. 85 ع. 13: 2797–800. Bibcode:2000PhRvL..85.2797E. DOI:10.1103/PhysRevLett.85.2797. PMID:10991236.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء عددية: قائمة المؤلفين (link) صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) صيانة الاستشهاد: علامات ترقيم زائدة (link) - ^ Christe, K. O.؛ Dixon, D. A.؛ Sanders, J. C. P.؛ Schrobilgen, G. J.؛ Tsai, S. S.؛ Wilson, W. W. (1995). "On the Structure of the [XeOF5]− Anion and of Heptacoordinated Complex Fluorides Containing One or Two Highly Repulsive Ligands or Sterically Active Free Valence Electron Pairs". Inorg. Chem. ج. 34 ع. 7: 1868–1874. DOI:10.1021/ic00111a039.
- ^ Williams، David R. (19 أبريل 2007). "Earth Fact Sheet". NASA. مؤرشف من الأصل في 2019-05-13. اطلع عليه بتاريخ 2007-10-04.
- ^ Cleveland, Z.I.; Möller, H.E.; Hedlund, L.W.; Driehuys, B. (2009). "Continuously infusing hyperpolarized 129Xe into flowing aqueous solutions using hydrophobic gas exchange membranes". The journal of physical chemistry. ج. 113 ع. 37: 12489–99. DOI:10.1021/jp9049582. PMC:2747043. PMID:19702286.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Gaede, H. C.; Song, Y. -Q.; Taylor, R. E.; Munson, E. J.; Reimer, J. A.; Pines, A. (1995). "High-field cross polarization NMR from laser-polarized xenon to surface nuclei". Applied Magnetic Resonance. ج. 8 ع. 3–4: 373. DOI:10.1007/BF03162652.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Finkel، A. J. (1 أبريل 1968). "Metabolic and toxicological effects of water-soluble xenon compounds are studied". NASA. مؤرشف من الأصل في 2019-05-03. اطلع عليه بتاريخ 2007-10-04.
{{استشهاد ويب}}: النص "0" تم تجاهله (مساعدة) والوسيط author-name-list parameters تكرر أكثر من مرة (مساعدة) - ^ Staff (1 أغسطس 2007). "Cryogenic and Oxygen Deficiency Hazard Safety". Stanford Linear Accelerator Center. مؤرشف من الأصل في 2007-06-09. اطلع عليه بتاريخ 2007-10-10.
| H | He | |||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
