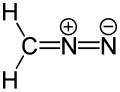
مركب ثنائي القطب
مركب ثنائي القطب في الكيمياء العضوية، مركب ثنائي القطب أو ببساطة ثنائي القطب هو جزيء محايد كهربائيا تحمل شحنة إيجابية وسلبية في وصف الكنسي واحد على الأقل. في معظم المركبات dipolar يتم delocalized التهم.[1] على عكس الأملاح، تحتوي المركبات الزَّينية على ذرات منفصلة، وليس على الأيونات الإيجابية والسلبية التي تشكل المركب. المركبات ثنائي القطب تظهر لحظة ثنائي القطب.
يمكن أن تكون ممثلة المركبات ثنائي القطب من قبل بنية الرنين. ويشار إلى الهياكل المساهمة التي تحتوي على ذرات مشحونة على أنها زويزتيريون.[2][3][4][5][6] يمكن أن يكون لبعض المركبات الزُينة شكلًا قانونيًا غير مشحون.
أنواع المركبات ثنائي القطب[عدل]
- 1،2-مركبات dipolar لها رسوم معاكسة على الذرات المجاورة.
- 1،3-مركبات dipolar قد التهم فصلت على ثلاث ذرات.[1] هم يتفاعلون في 1,3-dipolar cycloadditions.
- أيضا 1،4-dipolars،[4] 1،5-dipolars، وهلم جرا موجودة.
أمثلة[عدل]
-
ديازومثان
انظر أيضًا[عدل]
المراجع[عدل]
- ^ أ ب الاتحاد الدولي للكيمياء البحتة والتطبيقية. "dipolar compounds". Compendium of Chemical Terminology Internet edition.
- ^ Braida et al.: A clear correlation between the diradical character of 1,3-dipoles and their reactivity toward ethylene or acetylene.; J. Am. Chem. Soc.; 2010 Jun 9;132(22):7631-7 نسخة محفوظة 2 أغسطس 2020 على موقع واي باك مشين.
- ^ Hartmann and Heuschmann: Isolation of a Zwitterion in a Diels–Alder Reaction with Inverse Electron Demand; Angewandte Chemie; september 1989; Volume 28, Issue 9, pages 1267–1268 نسخة محفوظة 2012-11-02 على موقع واي باك مشين.
- ^ أ ب MacHiguchi، Takahisa؛ Okamoto، Junko؛ Takachi، Junpei؛ Hasegawa، Toshio؛ Yamabe، Shinichi؛ Minato، Tsutomu (2003). "Exclusive Formation of α-Methyleneoxetanes in Ketene−Alkene Cycloadditions. Evidence for Intervention of Both an α-Methyleneoxetane and the Subsequent 1,4-Zwitterion". Journal of the American Chemical Society. ج. 125 ع. 47: 14446–8. DOI:10.1021/ja030191g. PMID:14624592.
- ^ IUPAC: Preferred الاتحاد الدولي للكيمياء البحتة والتطبيقية Names; Chapter 7, September 2004, pp. 56-70 نسخة محفوظة 2017-11-18 على موقع واي باك مشين.
- ^ Rolf Huisgen (IUPAC): Cycloaddition mechanism and the solvent dependence of rate; Pure Appl. Chem.; 1980, Vol.52, pp.2283—2302. نسخة محفوظة 2017-12-01 على موقع واي باك مشين.