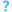مستخدم:عمر همام/ملعب الجرثومة
| عمر همام/ملعب الجرثومة | |
|---|---|
 Immunohistochemical staining of H. pylori (brown) from a gastric biopsy
| |
| تسميات أخرى | Campylobacter pylori |
| النطق | /ˈhɛlɪkoʊˌbæktər paɪˈlɔːraɪ, pɪ-, -ri/[1][2] |
| معلومات عامة | |
| الاختصاص | Infectious disease, gastroenterology |
| الأسباب | |
| الأسباب | Helicobacter pylori spread by fecal oral route[3] |
| المظهر السريري | |
| الأعراض | Hematemesis, Melena, abdominal pain, nausea[4][3] |
| المضاعفات | Gastritis, Stomach ulcer, stomach cancer |
| الإدارة | |
| التشخيص | Urea breath test, fecal antigen assay, tissue biopsy[3] |
| أدوية | |
| الوبائيات | |
| انتشار المرض | >50% (2015)[6] |
| تعديل مصدري - تعديل | |
| عمر همام/ملعب الجرثومة | |
|---|---|
 الصبغ الـ ابنسيجي الكيميائي المناعي لل" الملوية البوابية" (باللون البني) من خزعة مأخوذة من المعدة
| |
| تسميات أخرى | Campylobacter pylori "هيليكوباكتر بيلوري" "العَطيفَةُ البَوَّابِيَّة" "" |
| النطق | /ˈhɛlɪkoʊˌbæktər paɪˈlɔːraɪ, pɪ-, -ri/[7][8] |
| معلومات عامة | |
| الاختصاص | أمراض معدية (اختصاص طبي) , طب الجهاز الهضمي |
| الأسباب | |
| الأسباب | الملوية البوابية >> تنتشر عبر الطريق فموي-شرجي |
| المظهر السريري | |
| الأعراض | تقيؤ دموي, تغوط أسود, ألم بطني, غثيان[4][3] |
| المضاعفات | إلتهاب المعدة, قرحة المعدة, سرطان المعدة |
| الإدارة | |
| التشخيص | فحص الزفير باليوريا, فحص البراز, خزعة [3] |
| أدوية | |
| الوبائيات | |
| انتشار المرض | >50% (2015)[6] |
| تعديل مصدري - تعديل | |
الملوية البوابية (باللاتينية: Helicobacter pylori) أو جرثومة المعدة أو هيليكوباكتر بيلوري (بالإنجليزية: Helicobacter pylori) نوع من البكتيريا من العصيات سلبية الغرام أليفة الهواء القليل التي تستعمر مخاطيات المعدة[9] [5]و الإثنا عشر، مسببة التهاباً في المخاطية، وترتبط بتطور القرحات الهضمية في المعدة والإثنا عشر و سرطان المعدة. يبقى أكثر من 80% من المصابين بهذه الجرثومة بدون أي أعراض أو مضاعفات.
يحمل نحو 50% من سكان الأرض هذا الجرثوم، مما يجعله العدوى الأكثر انتشاراً في العالم[10]، وانتشاره أكبر في البلدان النامية منه في المتطورة. طريق العدوى غير معروف تماماً.
كانت تعرف سابقًا باسم العَطيفَةُ البَوَّابِيَّة (بالإنجليزية: Campylobacter pylori)، وهي لولبية (حلزونية)الشكل. يُعتقد أن شكلها الحلزوني (الذي اشتق منه اسم الجنس، الملوية (هيليكوباكتر)) قد تطور ليخترق الغشاء المخاطي للمعدة وبالتالي الإصابة بالعدوى.[11][12] تم التعرف على البكتيريا لأول مرة في عام 1982 من قبل الأطباء الأستراليين باري مارشال وروبن وارين.[13][14][15] تم ربط المَلْوِيَّة البَوَّابية بالأورام اللمفاوية للأنسجة اللمفاوية المرتبطة بالغشاء المخاطي في المعدة أو المريء أو القولون أو المستقيم أو الأنسجة المحيطة بالعين (يُطلق عليها سرطان الغدد الليمفاوية خارج الخلية في المنطقة الهامشية الخارجية للعضو المذكور)[بالإنجليزية]،[16] [17] والأنسجة اللمفاوية في المعدة (تسمى ورم الغدد الليمفاوية B- خلية كبيرة منتشرة). [18]
العلامات والأعراض[عدل]
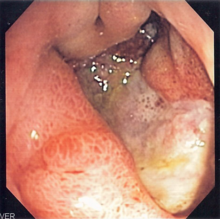
ما يصل إلى 90٪ من المصابين بالبكتيريا الملوية لا يعانون من أعراض أو مضاعفات.[19] ومع ذلك فإن الأفراد المصابين بالبكتيريا الملوية البوابية لديهم خطر على مدى حياتهم من 10٪ إلى 20٪ من الإصابة بالقرحة الهضمية.[20][21]
قد تظهر العدوى الحادة على شكل التهاب معوي حاد مصحوب بآلام في البطن (آلام في المعدة) أو غثيان.[4] عندما يتطور هذا إلى التهاب معوي مزمن، فإن الأعراض إن وجدت غالبًا ما تكون أعراض عسر الهضم غير القرحي: آلام في المعدة، والغثيان، والانتفاخ، والتجشؤ وفي بعض الأحيان القيء.[22][23] يحدث الألم عادةً عندما تكون المعدة فارغة وبين الوجبات وفي ساعات الصباح الباكر ولكن يمكن أن يحدث أيضًا في أوقات أخرى تشمل أعراض القرحة الأقل شيوعًا الغثيان والقيء وفقدان الشهية.
يمكن أن يحدث نزيف في المعدة أيضًا كما يتضح من مرور البراز الأسود قد يؤدي النزيف المطول إلى فقر الدم مما يؤدي إلى الضعف والإرهاق إذا كان النزيف شديدًا، فقد يحدث قيء دموي أو نزيف دموي أو ميلينا (تغوّط أسود اللون) من المرجح أن يؤدي التهاب غار البواب (بالانجليزية:pyloric antrum) الذي يربط المعدة بالاثني عشر إلى الإصابة بقرحة الاثني عشر بينما من المرجح أن يؤدي التهاب جسم المعدة إلى الإصابة بقرحة في المعدة.[24][25] قد يصاب الأفراد المصابون بالبكتيريا الملوية البوابية أيضًا بسَليلَة في القولون والمستقيم .[26][27] أو سليلة في المعدية.[28] والسلية عبارة عن نمو غير سرطاني للأنسجة البارزة من الأغشية المخاطية لهذه الأعضاء، وعادةً ما تكون هذه الأورام الحميدة بدون أعراض لكن السليلات الحميدة في المعدة قد تكون سببًا لعسر الهضم، وحرقة المعدة، والنزيف من الجهاز الهضمي العلوي، ونادرًا ما يؤدي إلى انسداد مخرج المعدة.[29] في حين أن السليلات الحميدة في القولون والمستقيم قد تكون سببًا لنزيف المستقيم، وفقر الدم، والإمساك، ,الإسهال ونقص الوزن وآلام البطن.[30]
الأفراد المصابون بعدوى الملوية البوابية المزمنة لديهم مخاطر متزايدة للإصابة بسرطان مرتبط مباشرة بهذه العدوى.[31][32][33][34] هذه السرطانات هي سرطان غدي في المعدة، وهو أقل شيوعًا انتشار سرطان الغدد الليمفاوية للخلايا B الكبيرة في المعدة.[35] أو الأورام اللمفاوية للخلايا B في المنطقة الهامشية خارج الغدة.[36][37] أو في حالات نادرة القولون.[38][39]المستقيم.[40] المريء.[41] أوالملحقات العينية[42] (بالإنجليزية: Ocular adnexa) (مثل محجر العين والملتحمة و / أو الجفون.[43][44]
الأحياء الدقيقة[عدل]
علم التشكل المورفولوجيا[عدل]
الملوية البوابية هي بكتيريا على شكل حلزوني (تصنف على أنها قضيب منحني، وليست البكتيريا الملتوية) و سلبية الغرام يبلغ طولها حوالي 3 ميكرون ويبلغ قطرها حوالي 0.5 ميكرومتر. يمكن للبكتيريا الملوية البابية أن تظهر في الأنسجة بواسطة صبغة غرام، صبغة جيمزا، صبغة الهيماتوكسيلين واليوزين، ملون وارثن-ستاري فضي اللون، صبغة الأكريدين أورانج،والفحص بالمجهر ضوئي ذو الأطوار المتباينة. إنها قادرة على تكوين أغشية حيوية [45] ويمكن أن يتحول من شكل حلزوني إلى شكل كروي قابل للحياة ولكنه غير قابل للزراعة. [46]
للملوية البوابية أربعة إلى ستة أسواط في نفس الموقع؛ جميع أنواع البكتيريا الموية المعوية والكبدية كثيرة الحركة بسبب الأسواط. تتكون الخيوط السوطية المغلفة المميزة للملوية من سوطين مشتركين، هما:FlaA و FlaB.[47]
علم وظائف الأعضاء[عدل]
الملوية البوابية هي جرثوم أليف الهواء القليل (ميكرويروفيليك) أي أنها تتطلب توافر الأكسجين، ولكن بتركيز أقل مما هو عليه في الغلاف الجوي. يحتوي على هيدروجيناز يمكنه إنتاج الطاقة عن طريق أكسدة الهيدروجين الجزيئي (H2) الذي تنتجه البكتيريا المعوية.[48] ينتج أوكسيديز ، كاتلاز ، ويورياز.
تمتلك الملوية بوابية خمس عائلات من البروتينات الغشائية الخارجية الرئيسية.[49] تضم العائلة الأكبر مواد لاصقة بكتيرية معروفة ومفترضة. والعائلات الأربع الأخرى هي البورينات، وناقلات الحديد، والبروتينات المرتبطة بالأسواط، والبروتينات غير معروفة الوظيفة. مثل غيرها من البكتيريا سالبة الجرام النموذجية ، يتكون الغشاء الخارجي للملوية البوابية من الدهن الفسفوري (فوسفوليبيد) وعديدات السكاريد الدهنية (LPS). قد يكون مستضد O (بالإنجليزية: O-Antigen) لـ LPS مسببًا للفوكوسيلات (بالإنجليزية:Fucose ) ويحاكي مستضدات فصيلة دم لويس الموجودة على النسيج الطلائي للمعدة.[49] يحتوي الغشاء الخارجي أيضًا على جلوكوزيدات الكوليسترول الموجودة في عدد قليل من أنواع البكتيريا الأخرى.
عمر همام/ملعب الجرثومة | |
|---|---|
| التصنيف العلمي | |
| الجنس: | Helicobacter |
| النوع: | pylori |
| تعديل مصدري - تعديل | |
العلاج[عدل]
التهاب المعدة[عدل]
التهاب المعدة السطحي، الحاد أو المزمن، هو أكثر أشكال عدوى الملوية البوابية شيوعًا تم العثور على علامات وأعراض هذا التهاب المعدة للتحول تلقائيا في العديد من الأفراد دون اللجوء إلى بروتوكولات القضاء على هيليكوباكتر بيلوري، تستمر العدوى البكتيرية بالبكتيريا الملوية البابية بعد الشفاء في هذه الحالات، يتم استخدام أنظمة دوائية مختلفة من المضادات الحيوية بالإضافة إلى مثبطات مضخة البروتون للقضاء على البكتيريا وبالتالي علاج الاضطراب بنجاح.[50] مع العلاج بالعقاقير الثلاثية التي تتكون من كلاريثروميسين وأموكسيسيلين (بالانجليرية: clarithromycin, amoxicillin) ومثبط مضخة البروتون التي تعطى لمدة 14-21 يومًا غالبًا ما يتم اعتبارها أولاً خط العلاج.[51]
القرحة الهضمية[عدل]
بمجرد اكتشاف بكتيريا الملوية البوابية في شخص مصاب بقرحة هضمية، فإن الإجراء الطبيعي هو استئصالها والسماح للقرحة بالشفاء، علاج الخط الأول القياسي هو "علاج ثلاثي" لمدة أسبوع واحد يتكون من مثبطات مضخة البروتون مثل أوميبرازول والمضادات الحيوية كلاريثروميسين وأموكسيسيلين.[52] (قد تعكس إجراءات مثبطات مضخة البروتون ضد الحلزونية البوابية تأثيرها المباشر للجراثيم بسبب تثبيط البكتيريا من النوع P-ATPase و / أو اليورياز.[53]) تم تطوير أشكال مختلفة من العلاج الثلاثي على مر السنين، مثل استخدام مثبط مختلف لمضخة البروتون، مثل البانتوبرازول أو الرابيبرازول، أو استبدال الأموكسيسيلين بالميترونيدازول للأشخاص الذين لديهم حساسية من البنسلين.[54] في المناطق ذات المعدلات الأعلى لمقاومة الكلاريثروميسين، يوصى بخيارات أخرى.[55] لقد أحدث هذا العلاج ثورة في علاج القرحة الهضمية وجعل علاج المرض ممكنًا. في السابق، كان الخيار الوحيد هو التحكم في الأعراض باستخدام مضادات الحموضة أو مضادات H2 أو مثبطات مضخة البروتون وحدها.[56][57]
مرض مقاوم للمضادات الحيوية[عدل]
تم العثور على عدد متزايد من الأفراد المصابين لإيواء البكتيريا المقاومة للمضادات الحيوية يؤدي هذا إلى فشل العلاج الأولي ويتطلب جولات إضافية من العلاج بالمضادات الحيوية أو استراتيجيات بديلة، مثل العلاج الرباعي الذي يضيف مادة غروانية البزموت مثل ساليسيلات البزموت.[58][59][60] لعلاج سلالات الحلزونية البوابية المقاومة للكلاريثروميسين تم اقتراح استخدام الليفوفلوكساسين كجزء من العلاج.[61][62]
يؤدي تناول بكتيريا حمض اللاكتيك إلى إحداث تأثير قمعي على عدوى الملوية البوابية في كل من الحيوانات والبشر كما أن تناول الزبادي المحتوي على بكتيريا Lactobacillus و Bifidobacterium قد أدى إلى تحسين معدلات القضاء على جرثومة الملوية البوابية في البشر.[63] تستخدم البكتيريا التكافلية المنتجة للزبدة والتي توجد عادة في الأمعاء أحيانًا كبروبيوتيك للمساعدة في قمع عدوى الملوية البوابية كعامل مساعد للعلاج بالمضادات الحيوية.[64] الزبدات نفسها هي مادة مضادة للميكروبات تدمر غلاف خلية الحلزونية البوابية عن طريق تحفيز التعبير التنظيمي للخلايا التائية (على وجه التحديد FOXP3) وتوليف ببتيد مضاد للميكروبات يسمى LL-37 ، والذي ينشأ من خلال عمله كمثبط هيستون ديستيلاز.[65][66]
تم اقتراح مادة سلفورافان التي توجد في البروكلي والقرنبيط كعلاج.[67][68][69] كما تم اقتراح علاج اللثة أو التحجيم وكشط الجذر كعلاج إضافي.[70]
السرطانات
الأورام اللمفاوية للخلايا B في المنطقة الهامشية الخارجية
المقال الرئيسي: سرطان الغدد الليمفاوية MALT
الأورام اللمفاوية للخلايا B في المنطقة الهامشية الخارجية (تسمى أيضًا أورام الغدد الليمفاوية MALT) هي بشكل عام أورام خبيثة بطيئة النمو العلاج الموصى به لورم الغدد الليمفاوية للخلايا B في المنطقة الهامشية الخارجية إيجابية الحلزونية البوابية عند توطينه (مثل المرحلة الأولى والثانية من آن أربور بالانجليزية:Ann Arbor stage I and II) يستخدم أحد أفواج مثبطات مضخة البروتون المضادات الحيوية المدرجة في بروتوكولات استئصال الحلزونية البوابية إذا فشل النظام العلاجي الأولي في القضاء على العامل الممرض يتم علاج المرضى ببروتوكول بديل يتم استئصال العامل الممرض بنجاح في 70-95٪ من الحالات.[71] حوالي 50-80 ٪ من المرضى الذين يختبرون استئصال العامل الممرض يتطورون في غضون 3-28 شهرًا إلى مغفرة وتحكم سريري طويل الأمد في الورم اللمفاوي كما تم استخدام العلاج الإشعاعي للمعدة والغدد الليمفاوية المحيطة (أي حول المعدة) لعلاج هذه الحالات الموضعية بنجاح المرضى الذين يعانون من مرض غير موضعي (مثل المرحلة الثالثة والرابعة من مرض آن أربور الجهازي) والذين لا يعانون من الأعراض قد عولجوا بالانتظار اليقظ أو إذا ظهرت عليهم الأعراض باستخدام عقار العلاج المناعي ريتوكسيماب (يُعطى لمدة 4 أسابيع) مع دواء العلاج الكيميائي كلورامبيوسيل لمدة 6-12 شهرًا 58٪ من هؤلاء المرضى يحققون معدل بقاء خالٍ من التقدم في الحياة بنسبة 58٪ عند 5 سنوات تم علاج مرضى المرحلة الثالثة / الرابعة بنجاح باستخدام ريتوكسيماب أو دواء العلاج الكيميائي سيكلوفوسفاميد بمفرده.[72] تم علاج الحالات النادرة فقط من سرطان الغدد الليمفاوية للخلايا B في المنطقة الحدية خارج الجسم إيجابية الحلزونية البوابية بنجاح باستخدام نظام مثبط لمضخة البروتون بالمضادات الحيوية العلاجات الموصى بها حاليًا لهذا المرض هي الاستئصال الجراحي أو الاستئصال بالمنظار أو الإشعاع أو العلاج الكيميائي أو مؤخرًا ريتوكسيماب.[73] في الحالات القليلة المبلغ عنها من سرطان الغدد الليمفاوية للخلايا B في المنطقة الهامشية الخارجية إيجابية الحلزونية البوابية في المريء تمت معالجة المرض الموضعي بنجاح باستخدام أنظمة مثبطات مضخة البروتون بالمضادات الحيوية ومع ذلك، فإن المرض المتقدم يبدو أقل استجابة أو غير مستجيب لهذه الأنظمة ولكنه يستجيب جزئيًا لريتوكسيماب تم استخدام العلاج باستئصال.[74] مثبطات مضخة البروتون والمضادات الحيوية والعلاج الإشعاعي الموضعي بنجاح في علاج الأورام اللمفاوية للخلايا B في المنطقة الحدية للخلايا الحلزونية البوابية الإيجابية في المستقيم ومع ذلك أعطى العلاج الإشعاعي نتائج أفضل قليلاً وبالتالي فقد تم اقتراحه ليكون العلاج المفضل للمرض.[75] حقق علاج سرطان الغدد الليمفاوية للخلايا B خارج المنطقة الحدية الموجبة من الحلزونية البوابية الموضعية في الغدة العينية مع أنظمة مثبطات المضادات الحيوية/ البروتون معدلات بقاء خالية من الفشل لمدة عامين و5 سنوات بنسبة 67 ٪ و55 ٪ على التوالي ومعدل تقدم بدون تقدم لمدة 5 سنوات بنسبة 61٪.[76]
ومع ذلك فإن العلاج المختار المعترف به عمومًا للمرضى الذين يعانون من تورط جهازي يستخدم العديد من أدوية العلاج الكيميائي غالبًا مع ريتوكسيماب.[77]
انتشار سرطان الغدد الخلايا الليمفاوية B الكبيرة
المقال الرئيسي: انتشار سرطان الغدد الليمفاوية للخلايا البائية الكبيرة
سرطان الغدد الليمفاوية للخلايا البائية B الكبيرة المنتشر هو سرطان أكثر عدوانية بكثير من سرطان الغدد الليمفاوية للخلايا البائية خارج النطاق.[78] قد تكون حالات هذا الورم الخبيث إيجابية الحلزونية البوابية من الورم الليمفاوي الأخير وهي أقل عدوانية وأكثر عرضة للعلاج من الحالات السلبية لبكتيريا الملوية البوابية.[79][80] تشير العديد من الدراسات الحديثة بقوة إلى أنه يمكن علاج سرطان الغدد الليمفاوية B-cell Lymphoma المنتشر في مرحلة مبكرة من بكتيريا Helicobacter pylori، عندما يقتصر على المعدة بنجاح باستخدام أنظمة مثبطات مضخة البروتون بالمضادات الحيوية.[81][82][83][84] ومع ذلك، تتفق هذه الدراسات أيضًا على أنه نظرًا لعدوانية ورم الغدد الليمفاوية للخلايا البائية الكبيرة المنتشرة، يجب اتباع المرضى الذين عولجوا بأحد أنظمة استئصال الحلزونية البوابية بعناية. إذا وجدت أنها لا تستجيب أو تتدهور سريريًا في هذه الأنظمة، فيجب تحويل هؤلاء المرضى إلى علاج أكثر تقليدية مثل العلاج الكيميائي (مثل CHOP أو نظام شبيه بـ CHOP) ، والعلاج المناعي (مثل ريتوكسيماب)، والجراحة، و/ أو العلاج الإشعاعي الموضعي.[85]
تم علاج ورم الغدد الليمفاوية للخلايا البائية الكبيرة المنتشرة إيجابية الحلزونية البوابية بنجاح باستخدام واحد أو مجموعة من هذه الطرق.[86]
سرطان المعدة
ترتبط بكتيريا Helicobacter pylori بمعظم حالات سرطان المعدة الغدي، خاصة تلك التي تقع خارج القلب في المعدة (مثل مفترق المريء والمعدة).[87] يعتبر علاج هذا السرطان عنيفًا للغاية مع علاج مرض موضعي بالتتابع بالعلاج الكيميائي والعلاج الإشعاعي قبل الاستئصال الجراحي.[88] نظرًا لأن هذا السرطان، بمجرد تطوره، يكون مستقلاً عن عدوى الملوية البوابية، لا يتم استخدام نظم مثبطات مضخة البروتون والمضادات الحيوية في علاجه.[89]
المصادر[عدل]
- ^ "Helicobacter". Merriam-Webster Dictionary., "pylori". Merriam-Webster Dictionary..
- ^ "pylori". Dictionary.com Unabridged. راندوم هاوس.
- ^ ا ب ج د ه و ز اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعCDC2015Tr - ^ ا ب ج Butcher، Graham P. (2003). Gastroenterology: An illustrated colour text. Elsevier Health Sciences. ص. 25. ISBN:978-0-443-06215-5.
- ^ ا ب ج Alfarouk KO، Bashir AH، Aljarbou AN، Ramadan AM، Muddathir AK، AlHoufie ST، وآخرون (22 فبراير 2019). "Helicobacter pylori in Gastric Cancer and Its Management". Frontiers in Oncology. ج. 9: 75. DOI:10.3389/fonc.2019.00075. PMC:6395443. PMID:30854333.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ ا ب Hooi JK، Lai WY، Ng WK، Suen MM، Underwood FE، Tanyingoh D، وآخرون (أغسطس 2017). "Global Prevalence of Helicobacter pylori Infection: Systematic Review and Meta-Analysis". Gastroenterology. ج. 153 ع. 2: 420–429. DOI:10.1053/j.gastro.2017.04.022. PMID:28456631.
- ^ "Helicobacter". Merriam-Webster Dictionary., "pylori". Merriam-Webster Dictionary..
- ^ "pylori". Dictionary.com Unabridged. راندوم هاوس.
- ^ "كل شئ عن بكتيريا المعدة وأنواعها". فواصل. 14 أبريل 2020. مؤرشف من الأصل في 2020-04-14. اطلع عليه بتاريخ 2020-04-15.
- ^ Pounder R.E., Ng D. (1995). "The prevalence of Helicobacter pylori infection in different countries". Aliment. Pharmacol. Ther. 9 Suppl 2: 33–9. PMID:8547526.
- ^ Yamaoka Y (2008). Helicobacter pylori: Molecular Genetics and Cellular Biology. Caister Academic Press. ISBN:978-1-904455-31-8.
- ^ Brown LM (2000). "Helicobacter pylori: epidemiology and routes of transmission". Epidemiologic Reviews. ج. 22 ع. 2: 283–97. DOI:10.1093/oxfordjournals.epirev.a018040. PMID:11218379.
- ^ Warren JR، Marshall B (يونيو 1983). "Unidentified curved bacilli on gastric epithelium in active chronic gastritis". Lancet. ج. 1 ع. 8336: 1273–5. DOI:10.1016/S0140-6736(83)92719-8. PMID:6134060.
- ^ Marshall BJ، Warren JR (يونيو 1984). "Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration". Lancet. ج. 1 ع. 8390: 1311–5. DOI:10.1016/S0140-6736(84)91816-6. PMID:6145023. S2CID:10066001.
- ^ Sweet، Melissa (2 أغسطس 1997). "Smug as a bug". The Sydney Morning Herald. اطلع عليه بتاريخ 2007-01-28.
- ^ Abbas H، Niazi M، Makker J (مايو 2017). "Mucosa-Associated Lymphoid Tissue (MALT) Lymphoma of the Colon: A Case Report and a Literature Review". The American Journal of Case Reports. ج. 18: 491–497. DOI:10.12659/AJCR.902843. PMC:5424574. PMID:28469125.
- ^ Nocturne G، Pontarini E، Bombardieri M، Mariette X (مارس 2019). "Lymphomas complicating primary Sjögren's syndrome: from autoimmunity to lymphoma". Rheumatology. Oxford, UK. DOI:10.1093/rheumatology/kez052. PMID:30838413.
- ^ Paydas S (أبريل 2015). "Helicobacter pylori eradication in gastric diffuse large B cell lymphoma". World Journal of Gastroenterology. ج. 21 ع. 13: 3773–6. DOI:10.3748/wjg.v21.i13.3773. PMC:4385524. PMID:25852262.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Bytzer P، Dahlerup JF، Eriksen JR، Jarbøl DE، Rosenstock S، Wildt S (أبريل 2011). "Diagnosis and treatment of Helicobacter pylori infection". Danish Medical Bulletin. ج. 58 ع. 4: C4271. PMID:21466771. مؤرشف من الأصل في 2014-01-05.
- ^ Chang AH، Parsonnet J (أكتوبر 2010). "Role of bacteria in oncogenesis". Clinical Microbiology Reviews. ج. 23 ع. 4: 837–57. DOI:10.1128/CMR.00012-10. PMC:2952975. PMID:20930075.
- ^ Kusters JG، van Vliet AH، Kuipers EJ (يوليو 2006). "Pathogenesis of Helicobacter pylori infection". Clinical Microbiology Reviews. ج. 19 ع. 3: 449–90. DOI:10.1128/CMR.00054-05. PMC:1539101. PMID:16847081.
- ^ Butcher 2003، صفحات 24–5
- ^ Ryan، Kenneth (2010). Sherris Medical Microbiology. McGraw-Hill. ص. 573, 576. ISBN:978-0-07-160402-4.
- ^ Wu Q، Yang ZP، Xu P، Gao LC، Fan DM (يوليو 2013). "Association between Helicobacter pylori infection and the risk of colorectal neoplasia: a systematic review and meta-analysis". Colorectal Disease. ج. 15 ع. 7: e352-64. DOI:10.1111/codi.12284. PMID:23672575. S2CID:5444584.
- ^ "Helicobacter pylori" (PDF). cdc.gov. Center for Disease Control. اطلع عليه بتاريخ 2017-10-07.
- ^ Wu Q، Yang ZP، Xu P، Gao LC، Fan DM (يوليو 2013). "Association between Helicobacter pylori infection and the risk of colorectal neoplasia: a systematic review and meta-analysis". Colorectal Disease. ج. 15 ع. 7: e352-64. DOI:10.1111/codi.12284. PMID:23672575. S2CID:5444584.
- ^ "Helicobacter pylori" (PDF). cdc.gov. Center for Disease Control. اطلع عليه بتاريخ 2017-10-07.
- ^ Markowski AR، Markowska A، Guzinska-Ustymowicz K (أكتوبر 2016). "Pathophysiological and clinical aspects of gastric hyperplastic polyps". World Journal of Gastroenterology. ج. 22 ع. 40: 8883–8891. DOI:10.3748/wjg.v22.i40.8883. PMC:5083793. PMID:27833379.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Markowski AR، Markowska A، Guzinska-Ustymowicz K (أكتوبر 2016). "Pathophysiological and clinical aspects of gastric hyperplastic polyps". World Journal of Gastroenterology. ج. 22 ع. 40: 8883–8891. DOI:10.3748/wjg.v22.i40.8883. PMC:5083793. PMID:27833379.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Soetikno RM، Kaltenbach T، Rouse RV، Park W، Maheshwari A، Sato T، وآخرون (مارس 2008). "Prevalence of nonpolypoid (flat and depressed) colorectal neoplasms in asymptomatic and symptomatic adults". JAMA. ج. 299 ع. 9: 1027–35. DOI:10.1001/jama.299.9.1027. PMID:18319413.
- ^ Nocturne G، Pontarini E، Bombardieri M، Mariette X (مارس 2019). "Lymphomas complicating primary Sjögren's syndrome: from autoimmunity to lymphoma". Rheumatology. Oxford, UK. DOI:10.1093/rheumatology/kez052. PMID:30838413.
- ^ Abbas H، Niazi M، Makker J (مايو 2017). "Mucosa-Associated Lymphoid Tissue (MALT) Lymphoma of the Colon: A Case Report and a Literature Review". The American Journal of Case Reports. ج. 18: 491–497. DOI:10.12659/AJCR.902843. PMC:5424574. PMID:28469125.
- ^ Chang AH، Parsonnet J (أكتوبر 2010). "Role of bacteria in oncogenesis". Clinical Microbiology Reviews. ج. 23 ع. 4: 837–57. DOI:10.1128/CMR.00012-10. PMC:2952975. PMID:20930075.
- ^ Kusters JG، van Vliet AH، Kuipers EJ (يوليو 2006). "Pathogenesis of Helicobacter pylori infection". Clinical Microbiology Reviews. ج. 19 ع. 3: 449–90. DOI:10.1128/CMR.00054-05. PMC:1539101. PMID:16847081.
- ^ Paydas S (أبريل 2015). "Helicobacter pylori eradication in gastric diffuse large B cell lymphoma". World Journal of Gastroenterology. ج. 21 ع. 13: 3773–6. DOI:10.3748/wjg.v21.i13.3773. PMC:4385524. PMID:25852262.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Schreuder MI، van den Brand M، Hebeda KM، Groenen PJ، van Krieken JH، Scheijen B (ديسمبر 2017). "Novel developments in the pathogenesis and diagnosis of extranodal marginal zone lymphoma". Journal of Hematopathology. ج. 10 ع. 3–4: 91–107. DOI:10.1007/s12308-017-0302-2. PMC:5712330. PMID:29225710.
- ^ Smedby KE، Ponzoni M (نوفمبر 2017). "The aetiology of B-cell lymphoid malignancies with a focus on chronic inflammation and infections". Journal of Internal Medicine. ج. 282 ع. 5: 360–370. DOI:10.1111/joim.12684. PMID:28875507. S2CID:42071521.
- ^ Abbas H، Niazi M، Makker J (مايو 2017). "Mucosa-Associated Lymphoid Tissue (MALT) Lymphoma of the Colon: A Case Report and a Literature Review". The American Journal of Case Reports. ج. 18: 491–497. DOI:10.12659/AJCR.902843. PMC:5424574. PMID:28469125.
- ^ Smedby KE، Ponzoni M (نوفمبر 2017). "The aetiology of B-cell lymphoid malignancies with a focus on chronic inflammation and infections". Journal of Internal Medicine. ج. 282 ع. 5: 360–370. DOI:10.1111/joim.12684. PMID:28875507. S2CID:42071521.
- ^ Kobayashi T، Takahashi N، Hagiwara Y، Tamaru J، Kayano H، Jin-nai I، وآخرون (يناير 2008). "Successful radiotherapy in a patient with primary rectal mucosa-associated lymphoid tissue lymphoma without the API2-MALT1 fusion gene: a case report and review of the literature". Leukemia Research. ج. 32 ع. 1: 173–5. DOI:10.1016/j.leukres.2007.04.017. PMID:17570523.
- ^ Ma Q، Zhang C، Fang S، Zhong P، Zhu X، Lin L، Xiao H (مارس 2017). "Primary esophageal mucosa-associated lymphoid tissue lymphoma: A case report and review of literature". Medicine. ج. 96 ع. 13: e6478. DOI:10.1097/MD.0000000000006478. PMC:5380272. PMID:28353588.
- ^ "Al-Qamoos القاموس - English Arabic dictionary / قاموس إنجليزي عربي". www.alqamoos.org. مؤرشف من الأصل في 2019-12-14. اطلع عليه بتاريخ 2018-06-27.
- ^ Guffey Johnson J، Terpak LA، Margo CE، Setoodeh R (أبريل 2016). "Extranodal Marginal Zone B-cell Lymphoma of the Ocular Adnexa". Cancer Control. ج. 23 ع. 2: 140–9. DOI:10.1177/107327481602300208. PMID:27218791.
- ^ Saccà SC، Vagge A، Pulliero A، Izzotti A (ديسمبر 2014). "Helicobacter pylori infection and eye diseases: a systematic review". Medicine. ج. 93 ع. 28: e216. DOI:10.1097/md.0000000000000216. PMC:4603085. PMID:25526440.
- ^ Stark RM، Gerwig GJ، Pitman RS، Potts LF، Williams NA، Greenman J، وآخرون (فبراير 1999). "Biofilm formation by Helicobacter pylori". Letters in Applied Microbiology. ج. 28 ع. 2: 121–6. DOI:10.1046/j.1365-2672.1999.00481.x. PMID:10063642. S2CID:8912327.
- ^ Chan WY، Hui PK، Leung KM، Chow J، Kwok F، Ng CS (أكتوبر 1994). "Coccoid forms of Helicobacter pylori in the human stomach". American Journal of Clinical Pathology. ج. 102 ع. 4: 503–7. DOI:10.1093/ajcp/102.4.503. PMID:7524304.
- ^ Rust M، Schweinitzer T، Josenhans C (2008). "Helicobacter Flagella, Motility and Chemotaxis". في Yamaoka, Y. (المحرر). Helicobacter pylori: Molecular Genetics and Cellular Biology. Caister Academic Press. ISBN:978-1-904455-31-8.
- ^ Olson JW، Maier RJ (نوفمبر 2002). "Molecular hydrogen as an energy source for Helicobacter pylori". Science. ج. 298 ع. 5599: 1788–90. Bibcode:2002Sci...298.1788O. DOI:10.1126/science.1077123. PMID:12459589. S2CID:27205768.
- ^ ا ب Kusters JG، van Vliet AH، Kuipers EJ (يوليو 2006). "Pathogenesis of Helicobacter pylori infection". Clinical Microbiology Reviews. ج. 19 ع. 3: 449–90. DOI:10.1128/CMR.00054-05. PMC:1539101. PMID:16847081.
- ^ Burkitt MD، Duckworth CA، Williams JM، Pritchard DM (فبراير 2017). "Helicobacter pylori-induced gastric pathology: insights from in vivo and ex vivo models". Disease Models & Mechanisms. ج. 10 ع. 2: 89–104. DOI:10.1242/dmm.027649. PMC:5312008. PMID:28151409.
- ^ Azer، S. A.؛ Akhondi، H. (2019). "Gastritis". StatPearls. PMID:31334970.
- ^ Malfertheiner P، Megraud F، O'Morain CA، Atherton J، Axon AT، Bazzoli F، وآخرون (European Helicobacter Study Group) (مايو 2012). "Management of Helicobacter pylori infection--the Maastricht IV/ Florence Consensus Report". Gut. ج. 61 ع. 5: 646–64. DOI:10.1136/gutjnl-2012-302084. PMID:22491499. S2CID:1401974.
- ^ Minalyan A، Gabrielyan L، Scott D، Jacobs J، Pisegna JR (أغسطس 2017). "The Gastric and Intestinal Microbiome: Role of Proton Pump Inhibitors". Current Gastroenterology Reports. ج. 19 ع. 8: 42. DOI:10.1007/s11894-017-0577-6. PMC:5621514. PMID:28733944.
- ^ Malfertheiner P، Megraud F، O'Morain C، Bazzoli F، El-Omar E، Graham D، وآخرون (يونيو 2007). "Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report". Gut. ج. 56 ع. 6: 772–81. DOI:10.1136/gut.2006.101634. PMC:1954853. PMID:17170018.
- ^ Malfertheiner P، Megraud F، O'Morain CA، Gisbert JP، Kuipers EJ، Axon AT، وآخرون (European Helicobacter and microbiota study group and consensus panel) (يناير 2017). "Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report". Gut. ج. 66 ع. 1: 6–30. DOI:10.1136/gutjnl-2016-312288. PMID:27707777. S2CID:52868868.
- ^ Rauws EA، Tytgat GN (مايو 1990). "Cure of duodenal ulcer associated with eradication of Helicobacter pylori". Lancet. ج. 335 ع. 8700: 1233–5. DOI:10.1016/0140-6736(90)91301-P. PMID:1971318. S2CID:41888935.
- ^ Graham DY، Lew GM، Evans DG، Evans DJ، Klein PD (أغسطس 1991). "Effect of triple therapy (antibiotics plus bismuth) on duodenal ulcer healing. A randomized controlled trial". Annals of Internal Medicine. ج. 115 ع. 4: 266–9. DOI:10.7326/0003-4819-115-4-266. PMID:1854110.
- ^ Stenström B، Mendis A، Marshall B (أغسطس 2008). "Helicobacter pylori--the latest in diagnosis and treatment". Australian Family Physician. ج. 37 ع. 8: 608–12. PMID:18704207.
- ^ Fischbach L، Evans EL (أغسطس 2007). "Meta-analysis: the effect of antibiotic resistance status on the efficacy of triple and quadruple first-line therapies for Helicobacter pylori". Alimentary Pharmacology & Therapeutics (Meta-analysis). ج. 26 ع. 3: 343–57. DOI:10.1111/j.1365-2036.2007.03386.x. PMID:17635369. S2CID:20973127.
- ^ Graham DY، Shiotani A (يونيو 2008). "New concepts of resistance in the treatment of Helicobacter pylori infections". Nature Clinical Practice. Gastroenterology & Hepatology. ج. 5 ع. 6: 321–31. DOI:10.1038/ncpgasthep1138. PMC:2841357. PMID:18446147.
- ^ Perna F، Zullo A، Ricci C، Hassan C، Morini S، Vaira D (نوفمبر 2007). "Levofloxacin-based triple therapy for Helicobacter pylori re-treatment: role of bacterial resistance". Digestive and Liver Disease. ج. 39 ع. 11: 1001–5. DOI:10.1016/j.dld.2007.06.016. PMID:17889627.
- ^ Hsu PI، Wu DC، Chen A، Peng NJ، Tseng HH، Tsay FW، وآخرون (يونيو 2008). "Quadruple rescue therapy for Helicobacter pylori infection after two treatment failures". European Journal of Clinical Investigation. ج. 38 ع. 6: 404–9. DOI:10.1111/j.1365-2362.2008.01951.x. PMID:18435764. S2CID:205290582.
- ^ Wang KY، Li SN، Liu CS، Perng DS، Su YC، Wu DC، وآخرون (سبتمبر 2004). "Effects of ingesting Lactobacillus- and Bifidobacterium-containing yogurt in subjects with colonized Helicobacter pylori". The American Journal of Clinical Nutrition. ج. 80 ع. 3: 737–41. DOI:10.1093/ajcn/80.3.737 (غير نشط 31 مايو 2021). PMID:15321816.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: وصلة دوي غير نشطة منذ 2021 (link) - ^ Franceschi F، Cazzato A، Nista EC، Scarpellini E، Roccarina D، Gigante G، وآخرون (نوفمبر 2007). "Role of probiotics in patients with Helicobacter pylori infection". Helicobacter. 12 Suppl 2 ع. Suppl 2: 59–63. DOI:10.1111/j.1523-5378.2007.00565.x. PMID:17991178. S2CID:21791620.
- ^ Yonezawa H، Osaki T، Hanawa T، Kurata S، Zaman C، Woo TD، وآخرون (أبريل 2012). "Destructive effects of butyrate on the cell envelope of Helicobacter pylori". Journal of Medical Microbiology. ج. 61 ع. Pt 4: 582–589. DOI:10.1099/jmm.0.039040-0. PMID:22194341.
- ^ McGee DJ، George AE، Trainor EA، Horton KE، Hildebrandt E، Testerman TL (يونيو 2011). "Cholesterol enhances Helicobacter pylori resistance to antibiotics and LL-37". Antimicrobial Agents and Chemotherapy. ج. 55 ع. 6: 2897–904. DOI:10.1128/AAC.00016-11. PMC:3101455. PMID:21464244.
- ^ Moon JK، Kim JR، Ahn YJ، Shibamoto T (يونيو 2010). "Analysis and anti-Helicobacter activity of sulforaphane and related compounds present in broccoli ( Brassica oleracea L.) sprouts". Journal of Agricultural and Food Chemistry. ج. 58 ع. 11: 6672–7. DOI:10.1021/jf1003573. PMID:20459098.
- ^ Fahey JW، Haristoy X، Dolan PM، Kensler TW، Scholtus I، Stephenson KK، وآخرون (مايو 2002). "Sulforaphane inhibits extracellular, intracellular, and antibiotic-resistant strains of Helicobacter pylori and prevents benzo[a]pyrene-induced stomach tumors". Proceedings of the National Academy of Sciences of the United States of America. ج. 99 ع. 11: 7610–5. Bibcode:2002PNAS...99.7610F. DOI:10.1073/pnas.112203099. PMC:124299. PMID:12032331.
- ^ Haristoy X، Angioi-Duprez K، Duprez A، Lozniewski A (ديسمبر 2003). "Efficacy of sulforaphane in eradicating Helicobacter pylori in human gastric xenografts implanted in nude mice". Antimicrobial Agents and Chemotherapy. ج. 47 ع. 12: 3982–4. DOI:10.1128/aac.47.12.3982-3984.2003. PMC:296232. PMID:14638516.
- ^ Ren Q، Yan X، Zhou Y، Li WX (فبراير 2016). "Periodontal therapy as adjunctive treatment for gastric Helicobacter pylori infection". The Cochrane Database of Systematic Reviews. ج. 2: CD009477. DOI:10.1002/14651858.CD009477.pub2. PMID:26852297.
- ^ Violeta Filip P، Cuciureanu D، Sorina Diaconu L، Maria Vladareanu A، Silvia Pop C (2018). "MALT lymphoma: epidemiology, clinical diagnosis and treatment". Journal of Medicine and Life. ج. 11 ع. 3: 187–193. DOI:10.25122/jml-2018-0035. PMC:6197515. PMID:30364585.
- ^ Bron D، Meuleman N (سبتمبر 2019). "Marginal zone lymphomas: second most common lymphomas in older patients". Current Opinion in Oncology. ج. 31 ع. 5: 386–393. DOI:10.1097/CCO.0000000000000554. PMID:31246587.
- ^ Abbas H، Niazi M، Makker J (مايو 2017). "Mucosa-Associated Lymphoid Tissue (MALT) Lymphoma of the Colon: A Case Report and a Literature Review". The American Journal of Case Reports. ج. 18: 491–497. DOI:10.12659/AJCR.902843. PMC:5424574. PMID:28469125.
- ^ Ma Q، Zhang C، Fang S، Zhong P، Zhu X، Lin L، Xiao H (مارس 2017). "Primary esophageal mucosa-associated lymphoid tissue lymphoma: A case report and review of literature". Medicine. ج. 96 ع. 13: e6478. DOI:10.1097/MD.0000000000006478. PMC:5380272. PMID:28353588.
- ^ Kobayashi T، Takahashi N، Hagiwara Y، Tamaru J، Kayano H، Jin-nai I، وآخرون (يناير 2008). "Successful radiotherapy in a patient with primary rectal mucosa-associated lymphoid tissue lymphoma without the API2-MALT1 fusion gene: a case report and review of the literature". Leukemia Research. ج. 32 ع. 1: 173–5. DOI:10.1016/j.leukres.2007.04.017. PMID:17570523.
- ^ Guffey Johnson J، Terpak LA، Margo CE، Setoodeh R (أبريل 2016). "Extranodal Marginal Zone B-cell Lymphoma of the Ocular Adnexa". Cancer Control. ج. 23 ع. 2: 140–9. DOI:10.1177/107327481602300208. PMID:27218791.
- ^ Sassone M، Ponzoni M، Ferreri AJ (2017). "Ocular adnexal marginal zone lymphoma: Clinical presentation, pathogenesis, diagnosis, prognosis, and treatment". Best Practice & Research. Clinical Haematology. ج. 30 ع. 1–2: 118–130. DOI:10.1016/j.beha.2016.11.002. PMID:28288706.
- ^ Casulo C، Friedberg J (2017). "Transformation of marginal zone lymphoma (and association with other lymphomas)". Best Practice & Research. Clinical Haematology. ج. 30 ع. 1–2: 131–138. DOI:10.1016/j.beha.2016.08.029. PMID:28288708.
- ^ Kuo SH، Yeh KH، Chen LT، Lin CW، Hsu PN، Hsu C، وآخرون (يونيو 2014). "Helicobacter pylori-related diffuse large B-cell lymphoma of the stomach: a distinct entity with lower aggressiveness and higher chemosensitivity". Blood Cancer Journal. ج. 4 ع. 6: e220. DOI:10.1038/bcj.2014.40. PMC:4080211. PMID:24949857.
- ^ Cheng Y، Xiao Y، Zhou R، Liao Y، Zhou J، Ma X (أغسطس 2019). "Prognostic significance of helicobacter pylori-infection in gastric diffuse large B-cell lymphoma". BMC Cancer. ج. 19 ع. 1: 842. DOI:10.1186/s12885-019-6067-5. PMC:6712724. PMID:31455250.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Paydas S (أبريل 2015). "Helicobacter pylori eradication in gastric diffuse large B cell lymphoma". World Journal of Gastroenterology. ج. 21 ع. 13: 3773–6. DOI:10.3748/wjg.v21.i13.3773. PMC:4385524. PMID:25852262.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Kuo SH، Yeh KH، Chen LT، Lin CW، Hsu PN، Hsu C، وآخرون (يونيو 2014). "Helicobacter pylori-related diffuse large B-cell lymphoma of the stomach: a distinct entity with lower aggressiveness and higher chemosensitivity". Blood Cancer Journal. ج. 4 ع. 6: e220. DOI:10.1038/bcj.2014.40. PMC:4080211. PMID:24949857.
- ^ Tsai HJ، Tai JJ، Chen LT، Wu MS، Yeh KH، Lin CW، وآخرون (يوليو 2020). "A multicenter prospective study of first-line antibiotic therapy for early-stage gastric mucosa-associated lymphoid tissue lymphoma and diffuse large B-cell lymphoma with histological evidence of mucosa-associated lymphoid tissue". Haematologica. ج. 105 ع. 7: e349–e354. DOI:10.3324/haematol.2019.228775. PMC:7327622. PMID:31727764.
- ^ Cheng Y، Xiao Y، Zhou R، Liao Y، Zhou J، Ma X (أغسطس 2019). "Prognostic significance of helicobacter pylori-infection in gastric diffuse large B-cell lymphoma". BMC Cancer. ج. 19 ع. 1: 842. DOI:10.1186/s12885-019-6067-5. PMC:6712724. PMID:31455250.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Kuo SH، Yeh KH، Chen LT، Lin CW، Hsu PN، Hsu C، وآخرون (يونيو 2014). "Helicobacter pylori-related diffuse large B-cell lymphoma of the stomach: a distinct entity with lower aggressiveness and higher chemosensitivity". Blood Cancer Journal. ج. 4 ع. 6: e220. DOI:10.1038/bcj.2014.40. PMC:4080211. PMID:24949857.
- ^ Cheng Y، Xiao Y، Zhou R، Liao Y، Zhou J، Ma X (أغسطس 2019). "Prognostic significance of helicobacter pylori-infection in gastric diffuse large B-cell lymphoma". BMC Cancer. ج. 19 ع. 1: 842. DOI:10.1186/s12885-019-6067-5. PMC:6712724. PMID:31455250.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Laird-Fick HS، Saini S، Hillard JR (أغسطس 2016). "Gastric adenocarcinoma: the role of Helicobacter pylori in pathogenesis and prevention efforts". Postgraduate Medical Journal. ج. 92 ع. 1090: 471–7. DOI:10.1136/postgradmedj-2016-133997. PMID:27222587. S2CID:20739020.
- ^ Badgwell B، Das P، Ajani J (أغسطس 2017). "Treatment of localized gastric and gastroesophageal adenocarcinoma: the role of accurate staging and preoperative therapy". Journal of Hematology & Oncology. ج. 10 ع. 1: 149. DOI:10.1186/s13045-017-0517-9. PMC:5558742. PMID:28810883.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Laird-Fick HS، Saini S، Hillard JR (أغسطس 2016). "Gastric adenocarcinoma: the role of Helicobacter pylori in pathogenesis and prevention efforts". Postgraduate Medical Journal. ج. 92 ع. 1090: 471–7. DOI:10.1136/postgradmedj-2016-133997. PMID:27222587. S2CID:20739020.
| عمر همام/ملعب الجرثومة في المشاريع الشقيقة: | |