كيمياء لاعضوية
تحتاج هذه المقالة إلى تهذيب لتتناسب مع دليل الأسلوب في ويكيبيديا. (سبتمبر 2022) |
| صنف فرعي من | |
|---|---|
| جزء من | |
| يمتهنه | |
| الموضوع |
| جزء من سلسلة مقالات حول |
| كيمياء لاعضوية |
|---|
 |
| بوابة الكيمياء |
تتعامل الكيمياء غير العضوية مع نظريات المركبات العضوية والعضوية الفلزية وسلوكها. يغطي هذا المجال المركبات الكيميائية غير الكربونية وهي مواد الكيمياء العضوية.
التمييز بين التخصصين بعيد كل البعد عن المطلق، ويوجد الكثير من التداخل الفرعي مع الكيمياء العضوية الفلزية. ولها تطبيقات في كل جانب من جوانب الكيمياء الصناعية بما في ذلك التحفيز وعلم المواد والأصباغ والمواد الخافضة للتوتر السطحي والطلاء والأدوية والوقود والزراعة.
تُظهر المركبات غير العضوية تنوعًا غنيًا
أ-يتميز ثنائي البوران بآصرة غير اعتيادية.
ب-يحتوي كلوريد السيزيوم على بنية بلورية نموذجية.
ج-Fp2 مركب عضوي فلزي.
د-يُستخدم السليكون بدءًا من زراعة الثدي إلى المعجون السيليكوني.
ر-فاز محفّز غرابز بجائزة نوبل 2005 لاكتشافه.
و-يُستخدم الزيوليت على نطاق واسع في المناخل الجزيئية.
ي-فاجأت أسيتات النحاس الثنائي المنظرين بنفاذية مغناطيسية.
المفاهيم الرئيسية
[عدل]الكثير من المركبات العضوية هي مركبات أيونية تتكون من أيونات موجبة وأيونات سالبة مرتبطة بأواصر أيونية كالأملاح، يتكون MgCl2 كلوريد المغنيزيوم من أيونات موجبة Mg+2 وأيونات سالبة Cl-، ويتكون NaO2 أكسيد الصوديوم من أيونات موجبة Na+ وأيونات سالبة O2-. في أي ملح تكون نسب الأيونات متساوية حيث تُلغى الشحنات الكهربائية بصورة يكون فيها المركب الكتلي متعادل كهربائياً.
الفئات المهمة للمركبات غير العضوية هي الأكاسيد والكربونات والكبريتات والهاليدات، تتميز المركبات غير العضوية بنقاط انصهار عالية. تكون الأملاح غير العضوية عادة موصلات رديئة في الحالة الصلبة، تضم مميزاتها المهمة الأخرى درجة انصهارها العالية وسهولة تبلورها.
وبينما تكون بعض الأملاح مثل NaCl سريعة الذوبان في الماء، فإن البعض الآخر مثل FeS غير ذائب في الماء.
أبسط تفاعل غير عضوي هو الإزاحة المزدوجة عندما تُستبدَل الأيونات عند مزج ملحين دون التغيير في حالة الأكسدة والاختزال.
يقلل أحد المتفاعلات المؤكسد من حالة الأكسدة الخاصة به.
تزيد حالة الأكسدة للمتفاعل الآخر (مادة الاختزال) فتكون النتيجة النهائية تبادلًا إلكترونيًا. يحصل التبادل الإلكتروني بصورة غير مباشرة أيضاً مثل ما يحدث في البطاريات، وهو مفهوم رئيسي في الكيمياء الكهربائية.
إذا احتوى أحد المتفاعلات على ذرات الهيدروجين يمكن أن يحدث تفاعل بواسطة تبادل البروتونات في الكيمياء حامض- قاعدة. يُطلق تعريف أكثر شمولية على أي نوع كيميائي قادر على الارتباط بأزواج إلكترونية وهو حامض لويس، بعكس ذلك يُطلق على أي جزيء يستطيع التبرع بزوج إلكتروني قاعدة لويس.
لتحسين تفاعلات حامض-قاعدة تأخذ نظرية HSAB في الاعتبار قابلية الاستقطاب وحجم الأيونات. توجد المركبات غير العضوية بهيئة معادن، قد تحتوي التربة على كبريتيد الحديد مثل البيريت أو كبريتات الكالسيوم مثال الجبس. عُثِر على المركبات غير العضوية متعددة المهام مثل الجزيئات الحيوية الأكتروليت (NaCl كلوريد الصوديوم) في تخزين الطاقة (ATP)، أو في البناء في الحمض النووي DNA.
أول مركب عضوي صنعهُ الإنسان هو نترات الأمونيوم لتخصيب التربة من خلال عمليه Haber. تُصنع المركبات العضوية التي تُستخدم في هيئة محفزات مثل أكاسيد الفناديوم (V) وكلوريد التيتانيوم (lll) وكذلك كواشف في الكيمياء العضوية مثل هيدريد ألومنيوم الليثيوم. الأقسام الفرعية في الكيمياء غير العضوية هي الكيمياء العضوية الفلزية والكيمياء العنقودية والكيمياء غير العضوية الحياتية. تُعد هذه المجالات نشطة للبحث، تهدف الكيمياء غير العضوية إلى محفزات جيدة، موصلات فائقة، وعلاجات عديدة.
الكيمياء الصناعية غير العضوية
[عدل]يمكن تصنيف المركبات الغيرعضوية الصناعية تبعا لقابلية الذوبان والتطاير.[1] وفقا لإحصائيات 2005 تعتبر أشهر المركبات اللاعضوية التي يمكن صناعتها في كل من كندا، أوروبا، الصين، اليابان والولايات المتحدة كمايلي: كبريتات الألمنيوم، الامونيا، نيترات الأمونيوم، كبريتات الأمونيوم، أسود الكربون، الكلور، حمض الهيدروكلوريك، الهيدروجين، بيروكسيد الهيدروجين، حامض النتريك، النتروجين، الاوكسجين، حمض الفسفوريك، كربونات الصوديوم،كلورات الصوديوم، هيدروكسيد الصوديوم، سيليكات الصوديوم، كبريتات الصوديوم، حمض الكبريتيك، وأكسيد التيتانيوم. الكيمياء غير العضوية هي مجال عملي للغاية، تقليدياً يُقيَّم حجم اقتصاد الدولة من خلال إنتاجيتها لحامض الكبريتيك. يعتبر تصنيع الأسمدة الذي يبدأ غالبًا بعملية Haber-Bosch، تطبيقًا عمليًا آخر للكيمياء الصناعية غير العضوية.
تفاعلات كيميائية غير عضوية
[عدل]تلعب التفاعلات غير العضوية دورا كبيرا في الكيمياء. ومن أهم تلك التفاعلات تفاعل أكسدة-اختزال وهي تتم في تفاعل حامض-قاعدة. وتتم كل تلك التفاعلات تحت ظروف توازن كيميائي، إلا ان توازن التفاعل يكون فيها منحازا لأحد طرفي التفاعل الكيميائي وينتج عنه انثالبي التعادل الكيميائي كبير (حرارة شديدة).
لهذا نجد أن التفاعلات غير العضوية تسري سريعا وتنتج نواتجا وفيرة. وهذا بعكس التفاعلات العضوية فهي تسير ببطء حتى يصل التفاعل إلى حالة التوازن، والتي لا ينتج منها إلا نواتج قليلة.
خلال تفاعل أكسدة-اختزال ينتقل إلكترون أو أكثر من أحد المواد الداخلة في التفاعل إلى أحد المواد الأخرى الداخلة في التفاعل ويتفاعلان. في تفاعلات الأكسدة-اختزال يتم تفاعل بين عناصر منفردة وينتج منها مركبات. ومن أشهر تلك التفاعلات التفاعل الانفجاري وهو يتم باتحاد الهيدروجين مع الأكسجين بشدة وينتج الماء، وتفاعلات تأكسد تحدث مع العناصر غير النبيلة مثل الحديد حيث يتفاعل مع الأكسجين.
وفي تفاعل حامض-قاعدة (مثل تفاعل حامض الهيدروكلوريك مع الصوديوم أو هيدروكسيد الصوديوم) ينتقل بروتون بينهما، حيث تيعطي جزيء الحمض بروتونا (أيون هيدروجين ) إلى الصوديوم. ويتكون في معظم تفاعلات حمض-قلوي الماء وملح، وأشهرها تفاعل حمض الهيدروكلوريك مع هيدروكسيد الصوديوم فينتج ملح الطعام والماء. ونظرا لأن تلك التفاعلات تتم سريعا ويمكن فحصها بمؤشرات كيميائية فإنها ذات دور هام في الكيمياء التحليلية.
ويعتبر تكوين نواتج صلبة أو غازات خلال تفاعل كيميائي لا عضوي من العوامل التي تدفع بالتفاعل إلى السير بسرعة في اتجاه واحد حتى تكتمل، ذلك لأن النواتج تنفصل عن التوازن الكيميائي في المحلول ويتم التفاعل بذلك في اتجاه واحد فيكتمل.
لذلك فعند إضافة محلول كلوريد الباريوم مع محلول كبريتات الصوديوم فإن الناتج وهو كبريتات الباريوم تنفصل عن المحلول وتترسب، بسبب صعوبة ذوبانها في الماء. لهذا يتم هذا التفاعل بالكامل.
مثال :
مثال لتفاعل توازن يتم في اتجاه واحد نجده في تفاعل كلوريد الأمونيوم مع هيدروكسيد الصوديوم حيث ينتج غاز الأمونيا ويترك المحلول :
تلعب تلك التفاعلات دورا هاما في الكيمياء التحليلية.
تتحلل بعض المركبات غير العضوية عند ارتفاع درجة الحرارة منتجة غازات تنفصل عنها. ومن تلك الأمثلة مثال صناعة الجبس من الجص حيث يتحول كربونات الكالسيوم في المحمصة إلى أكسيد الكالسيوم ويتطاير غاز ثاني أكسيد الكربون.
بعد تكسير الجص إلى قطع صغيرة يرسل إلى التحميص ويوضع في الفرن عند درجة حرارة نحو 130 درجة مئوية ويبقى في الفرن لفترة كافية ريثما يـُطرد 3/4 الماء الذي بداخله، فتصبح صيغته الكيميائية: CaSO4.1/2H2O طبقا للتفاعل :
CaSO4.2H2O+حرارة = CaSO4.1/2H2O+1.5H2O
اتجاه سير التفاعل من اليمين إلى اليسار. ويتم كاملا نظرا لانفصال الماء وتبخره.
الكيمياء اللاعضوية الوصفية
[عدل]تهتم الكيمياء اللاعضوية الوصفية بتصنيف المركبات العضوية بناء على خواصها. من هذه التصنيفات:
المركبات التناسقية، Coordination compounds
[عدل]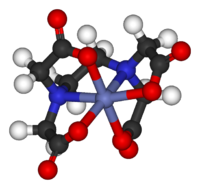
- مركبات العناصر الانتقالية، Transition metal compounds
- المركبات العنقودية، Cluster compounds
- المركبات العضوي الفلزية، Organometallic compounds
- المركبات اللاعضوية الحيوية، Bioinorganic compounds
- مركبات الحالة الصلبة، Solid state compounds
الكيمياء اللاعضوية النظرية
[عدل]تبدأ الكيمياء اللاعضوية النظرية من دراسة نموذج بور للذرة وباستخدام الكيمياء النظرية والكيمياء الحسابية يمكن بناء جزيئات بسيطة وأخرى معقدة.[3]
من أهم النظريات في الكيمياء اللاعضوية النظرية:
- نظريات كيفية Qualitative theories
- نظرية مجموعة التماثل الجزيئي Molecular symmetry group theory
الكيمياء اللاعضوية الميكانيكية
[عدل]- عناصر المجموعة الرئيسية واللانثانيدات Main group elements and lanthanides
- العناصر الانتقالية العقدية Transition metal complexes
وصلات داخلية
[عدل]المراجع
[عدل]- ^ "Facts & Figures Of The Chemical Industry” Chemical and Engineering News, July 10, 2006.
- ^ Lehn, J. M. (1995). Supramolecular Chemistry: Concepts and Perspectives. Weinheim: VCH.
- ^ Girolami, G.S.؛ Rauchfuss, T.B.؛ Angelici, R.J. (1999). Synthesis and Technique in Inorganic Chemistry (ط. 3rd). Mill Valley, CA: University Science Books. ISBN:978-0-935702-48-4.


