مرض رئوي خلالي
| مرض رئوي خلالي | |
|---|---|
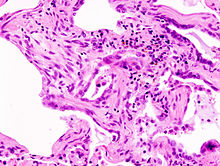
مرض رئوي خلالي - يثمثل في رئة شبيهة بعش النحل
| |
| معلومات عامة | |
| الاختصاص | طب الرئة |
| من أنواع | مرض رئوي ، والتهاب رئوي حاد، ومرض الرئة السنخي، ومرض النسيج الضام، ومرض |
| المظهر السريري | |
| الأعراض | التهاب[1] |
| الإدارة | |
| أدوية | |
| تعديل مصدري - تعديل | |
المرض الرئوي الخلالي (بالإنجليزية: Interstitial lung disease) او مرض مَتْن الرِّئَة المنتشر (DPLD) (بالإنجليزية: diffuse parenchymal lung disease)، يشير إلى مجموعة من الأمراض الرئوية التي تصيب النسيج الخلالي الرئوي (النسيج والفراغ حول الحويصلات الهوائية الرئوية).[2]يشمل ظهارة الحويصلات الهوائية، وبطانة الشعيرات الدموية الرئوية، والغشاء القاعدي، والأنسجة حول الأوعية واللمف المحيطي. قد يحدث عندما تؤدي إصابة الرئتين إلى استجابة شفاء غير طبيعية. في العادة، يُنتج الجسم الكمية المناسبة فقط من الأنسجة لإصلاح الضرر، ولكن في مرض الرئة الخلالي، تتعطل عملية الإصلاح، ويصبح النسيج المحيط بالأكياس الهوائية (الحويصلات الهوائية) متندبًا وسميكًا. هذا يجعل من الصعب على الأكسجين الانتقال إلى مجرى الدم. يظهر المرض بالأعراض التالية: ضيق التنفس، والسعال الجاف، والتعب، وفقدان الوزن، والتي تميل إلى التطور ببطء، على مدى عدة أشهر. متوسط معدل البقاء على قيد الحياة لشخص مصاب بهذا المرض يتراوح بين ثلاث وخمس سنوات. يُستخدم مصطلح ILD لتمييز هذه الأمراض عن أمراض الرئة المسدودة.[3][4]
هناك أنواع محددة لدى الأطفال، تُعرف باسم أمراض الرئة الخلالية عند الأطفال. يُستخدم الاختصار ChILD أحيانًا لهذه المجموعة من الأمراض. عند الأطفال، تشمل الفيزيولوجيا المرضية مكونًا وراثيًا، أو إصابة مرتبطة بالتعرض، أو خلل في المناعة الذاتية، أو جميع المكونات.[5][6]
يُصاب 30 إلى 40٪ من المصابين بمرض الرئة الخلالي في النهاية بالتليف الرئوي الذي يبلغ متوسط البقاء على قيد الحياة فيه 2.5-3.5 سنوات. التليف الرئوي مجهول السبب هو مرض رئوي خلالي لا يمكن تحديد سبب واضح له (مجهول السبب) ويرتبط بنتائج نموذجية لكل من التصوير الشعاعي (التليف القاعدي والمرتكز على الجنبة المنخربة) والمرضي (التليف غير المتجانس زمانيًا ومكانيًا، والتخرب النسيجي المرضي، وبؤر الأرومة الليفيَّة).[7]
في عام 2015، أثر مرض الرئة الخلالي، جنبًا إلى جنب مع الساركويد الرئوي، على 1.9 مليون شخص. وأدّت هذه الأمراض إلى 122 ألف حالة وفاة.[8]
الأسباب
[عدل]المرض الرئوي الخلالي يمكن تصنيفه الى ما إذا كان سببها غير معروف (مجهول السبب) أو معروف (ثانوي):[9]

مجهول السبب
[عدل]الألتهاب الرئوي الخلالي مجهول السبب هو المصطلح الذي يُطلق على أمراض الرئة الخلالية ذات السبب غير المعروف. وهي تمثل غالبية حالات أمراض الرئة الخلالية (ما يصل إلى ثلثي الحالات). وقد صُنفت فرعيًا من قبل الجمعية الأمريكية لطب الصدر في عام 2002 إلى 7 مجموعات فرعية:[10][11]
- التليف الرئوي مجهول السبب (IPF): المجموعة الفرعية الأكثر شيوعًا، حيث تمثل أكثر من 30٪ من أمراض الرئة الخلالية
- الالتهاب الرئوي الخلالي التوسفي (DIP)
- الالتهاب الرئوي الخلالي الحاد (AIP): يُعرف أيضًا باسم متلازمة هامان-ريتش
- الالتهاب الرئوي الخلالي غير النوعي (NSIP)
- التهاب القصيبات التنفسي الرئوي الخلالي (RB-ILD)
- الالتهاب الرئوي المنظم الخفي (COP): يُعرف أيضًا بالاسم القديم التهاب القصيبات المسدّ للالتهاب الرئوي المنظم (BOOP)
- الالتهاب الرئوي الخلالي اللمفاوي (LIP)
الثانوية
[عدل]أمراض الرئة الخلالية الثانوية هي تلك الأمراض التي لها سبب معروف، بما في ذلك:
النسيج الضام وأمراض المناعة الذاتية
[عدل]يمثل المرض المرتبط بالنسيج الضام ما يقرب من 25٪ من جميع حالات مرض الرئة الخلالي.
- داء الساركويد
- التهاب المفاصل الروماتويدي
- الذئبة الحمامية الشاملة
- تصلب الجلد المجموعي
- التهاب العضلات
- التهاب العضلات والجلد
- متلازمة مكافحة التخليق
المواد المستنشقة (تغبر الرئة)
[عدل]- غير عضوي
- السحار السيليسي
- داء الأسبست
- التسمم بالبيريليوم
- المواد الكيميائية المستخدمة في الطباعة الصناعية (مثل أسود الكربون، وضباب الحبر)
- عضوي
- التهاب فرط التحسس الرئوي (التهاب للحويصلات الهوائية الموجودة في الرئة بسبب الحساسية الزائدة لغبار المواد العضوية)، يمثل حوالي 15% من حالات مرض الرئة الخلالي.
ناتج عن الأدوية
[عدل]- المضادات الحيوية (على سبيل المثال، النيتروفورانتوين وعقاقير السلفا)
- العلاج الكيميائي
- مضادات اضطراب النظم
- ستاتين
- التدخين[12]
- التليف الخلالي المرتبط بالتدخين [الإنجليزية] (SRIF) هو مثال على نوع من أمراض الرئة الخلالية المعروفة بأنها ناجمة عن التدخين.
بسبب العدوى
[عدل]- مرض فيروس كورونا 2019 (كوفيد 19)[13]
- التهاب رئوي لانموذجي
- ذات الرئة بالمتكيسة الجؤجؤية
- السل
- المتدثرة التراخومية
- فيروس مخلوي تنفسي
بسبب السرطان
[عدل]مرض الرئة الخلالي عند الأطفال ومرض الرئة الخلالي بشكل رئيسي عند الأطفال
[عدل]- اضطرابات النمو المنتشرة
- شذوذ النمو وعوز التنسج السنخي
- حالات الرضع ذات السبب غير المحدد
- مرض الرئة الخلالي المتعلق بمنطقة الفاعل بالسطح السنخي[14]
التشخيص
[عدل]البحث مصمم وفقًا للأعراض والعلامات. إن التاريخ الصحيح والمفصل الذي يبحث عن التعرض المهني، وعن علامات الحالات المذكورة أعلاه هو الجزء الأول وربما الأهم من العمل في المرضى الذين يعانون من مرض الرئة الخلالي. عند الفحص، تُعدّ كراكر الفيلكرو، حيث تُقارن الكراكر بصوت فتح شريط الفيلكرو، شائعة في مرض الرئة الخلالي. تُظهر اختبارات وظائف الرئة عادةً عيبًا تقييديًا مع انخفاض قدرة انتشار أول أكسيد الكربون (DLCO) مما يشير إلى انخفاض انتقال الغازات من الحويصلات الهوائية إلى الشعيرات الدموية. يُشار إلى اختبار وظائف الرئة لجميع الأشخاص المصابين بمرض الرئة الخلالي، والتي يُعدّ فقدان حجم الهواء الكلي في الرئة (FVC) وانخفاض قدرة انتشار أول أكسيد الكربون مؤشرًا إنذاريًا لها، حيث يرتبط فقدان حجم الهواء الكلي في الرئة بأكثر من 5٪ سنويًا بتشخيص سيئ في الأنواع الفرعية الليفية من مرض الرئة الخلالي.[15]
يتمتع التصوير بالأشعة السينية للصدر بحساسية 63٪ وخصوصية 93٪ لمرض الرئة الخلالي. مع التقدم في التصوير المقطعي المحوسب، حلّت فحوصات التصوير المقطعي للصدر محل خزعة الرئة كاختبار تشخيصي مفضل لمرض الرئة الخلالي. يتمتع التصوير المقطعي للصدر بحساسية 91٪ وخصوصية 71٪ لمرض الرئة الخلالي. في البلدان ذات الدخل المرتفع، يخضع أقل من 10٪ من المصابين بمرض الرئة الخلالي لخزعة من الرئة كجزء من التقييم التشخيصي.[16]
يلزم أخذ خزعة من الرئة إذا لم يكن التاريخ السريري والتصوير يوحيان بوضوح بتشخيص محدد أو لا يمكن استبعاد الورم الخبيث. ترتبط خزعة الرئة الجراحية أو عن طريق خزعة جراحية بمساعدة الفيديو بالتنظير الصدري (VATS) بمعدل وفيات يصل إلى 1-2٪. ترتبط الخزعة المِجمدة عبر القصبات الهوائية بتنظير القصبات، حيث تُدخل كاميرا في الممرات الهوائية يتبعها تجميد سريع لمنطقة من أنسجة الرئة قبل الخزعة، بمعدل مضاعفات أقل ومعدل وفيات أقل بكثير مقارنة بخزعة VATS أو الخزعة الجراحية مع دقة تشخيصية قابلة للمقارنة تقريبًا. هناك أربعة أنواع من الأنماط النسيجية المرضية التي تُرى في مرض الرئة الخلالي: الالتهاب الرئوي الخلالي المعتاد، والالتهاب الرئوي الخلالي اللانوعي، والالتهاب الرئوي المنظم، وتلف الحويصلات الهوائية المنتشر. هناك تداخل كبير بين السمات النسيجية المرضية والإشعاعية لكل نوع من أنواع مرض الرئة الخلالي مما يجعل التشخيص صعبًا؛ حتى مع خزعة الرئة، لا يمكن تصنيف 15٪ من حالات مرض الرئة الخلالي.[17][18]
الأشعة السينية
[عدل]عادةً ما يكون التصوير الشعاعي للصدر هو أول اختبار للكشف عن أمراض الرئة الخلالية، ولكن يمكن أن يكون التصوير الشعاعي للصدر طبيعيًا في ما يصل إلى 10٪ من المرضى، خاصةً في وقت مبكر من عملية المرض.[19]
التصوير المقطعي المحوسب عالي الدقة للصدر هو الطريقة المفضلة، ويختلف عن التصوير المقطعي الروتيني للصدر. يفحص صندوق التصوير المقطعي المحوسب التقليدي (العادي) شرائح مقاس 7-10 مم يحصل عليها على فترات 10 مم؛ يفحص التصوير المقطعي عالي الدقة شرائح 1-1.5 مم بفواصل زمنية 10 مم باستخدام خوارزمية إعادة بناء عالية التردد المكاني. لذلك، يوفر التصوير المقطعي المحوسب عالي الدقة دقة أكثر بنحو 10 مرات من صندوق التصوير المقطعي المحوسب التقليدي، ما يسمح للتصوير المقطعي المحوسب عالي الدقة باستنباط تفاصيل لا يمكن تصورها بطريقة أخرى.[20]
ومع ذلك، فإن المظهر الإشعاعي وحده غير كافٍ ويجب تفسيره في السياق السريري، مع الأخذ في الاعتبار المظهر الزمني لعملية المرض.
يمكن تصنيف أمراض الرئة الخلالية وفقًا للأنماط الإشعاعية.[21]
نمط التعتيم
[عدل]التوحيد
حاد: متلازمات النزف السنخي، الالتهاب الرئوي الحاد اليوزيني، الالتهاب الرئوي الخلالي الحاد، الالتهاب الرئوي المنظم المشفر
مزمن: الالتهاب الرئوي اليوزيني المزمن، الالتهاب الرئوي المنظم، اضطرابات التكاثر اللمفاوي، البروتينات السنخية الرئوية، الساركوئيد
عتامات خطية أو شبكية
حاد: وذمة رئوية
مزمن: التليف الرئوي مجهول السبب، وأمراض الرئة الخلالية المرتبطة بالنسيج الضام، والأسبست، والساركوئيد، والتهاب الرئة المفرط الحساسية، وأمراض الرئة الناتجة عن الأدوية
عقيدات صغيرة
حاد: التهاب رئوي فرط الحساسية
مزمن: التهاب رئوي فرط الحساسية، الساركوئيد، السحار السيليسي، التهاب الرئة لدى عمال الفحم، التهاب القصيبات التنفسي، التحص المكروي السنخي
الأجواء الكيسية
مزمن: كثرة المنسجات لخلايا لانجرهان الرئوية، ورم عضلي وعائي لمفي رئوي، ورئة قرص العسل التي تسببها IPF أو أمراض أخرى
عتامة الزجاج الأرضي
حاد: متلازمات النزف السنخي، وذمة رئوية، والتهاب رئوي فرط الحساسية، والتعرض الاستنشاقي الحاد، وأمراض الرئة الناجمة عن الأدوية، والالتهاب الرئوي الخلالي الحاد
مزمن: الالتهاب الرئوي الخلالي غير النوعي، والتهاب القصيبات التنفسي المرتبط بأمراض الرئة الخلالية، والالتهاب الرئوي الخلالي التقشري، وأمراض الرئة الناجمة عن الأدوية، والبروتينات السنخية الرئوية
سماكة في الحاجز السنخي
حاد: وذمة رئوية[21]
مزمن: السرطان اللمفاوي، داء البروتينات السنخية الرئوية، الساركوئيد، مرض انسداد الوريد الرئوي
التوزيع
[عدل]غلبة الرئة العلوية
كثرة المنسجات لخلايا لانجرهانز الرئوية، السحار السيليسي، التهاب الرئة في عمال الفحم، التليف الرئوي المرتبط بالكارموستين، التهاب القصبات التنفسية المرتبط بمرض الرئة الخلالي.
هيمنة الرئة السفلية
التليف الرئوي مجهول السبب، التليف الرئوي المرتبط بأمراض النسيج الضام، الأسبست، الطموح المزمن
غلبة مركزية (محيط)
الساركوئيد، البريليوس
الهيمنة المحيطية
التليف الرئوي مجهول السبب، الالتهاب الرئوي اليوزيني المزمن، الالتهاب الرئوي المنظم المشفر
النتائج المرتبطة
[عدل]الانصباب الجنبي أو سماكة
الوذمة الرئوية، وأمراض النسيج الضام، والتليف الرئوي، والسرطان اللمفاوي، والورم الليمفاوي، والورم العضلي الوعائي اللمفاوي، وأمراض الرئة الناتجة عن الأدوية
تضخم العقد اللمفية
الساركوئيد، والسحار السيليسي، والسرطان اللمفاوي، والورم الليمفاوي، والالتهاب الرئوي الخلالي اللمفاوي
الاختبارات الجينية
[عدل]تم تحديد الأسباب الجينية لبعض أنواع أمراض أمراض الأطفال المزمنة (أمراض الرئة الخلالية) لدى الأطفال وبعض أشكال أمراض الشرايين التاجية للبالغين. يمكن تحديدها عن طريق اختبارات الدم. بالنسبة لعدد محدود من الحالات، فهذه ميزة أكيدة، حيث يمكن إجراء تشخيص جزيئي دقيق؛ في كثير من الأحيان ليست هناك حاجة لأخذ خزعة من الرئة.
الاختبار متاح لـ
أمراض الرئة الخلالية المتعلقة بالمنطقة السطحية السنخية
[عدل]نقص الفاعل بالسطح - البروتين - ب (الطفرات في SFTPB)
نقص الفاعل بالسطح - بروتين سي (الطفرات في SFTPC)
نقص ABCA3 (الطفرات في ABCA3)
متلازمة الغدة الدرقية الرئة في الدماغ (الطفرات في TTF1)
البروتينات السنخية الرئوية الخلقية (الطفرات في CSFR2A ، CSFR2B)
اضطراب النمو المنتشر
[عدل]خلل التنسج الشعري السنخي (الطفرات في FoxF1)
التليف الرئوي مجهول السبب
[عدل]الطفرات في إنزيم التيلوميراز العكسي (TERT)
الطفرات في مكون تيلوميراز RNA (TERC)
الطفرات في منظم استطالة التيلومير هيليكاز 1 (RTEL1)
الطفرات في بولي نوكلياز محدد (PARN)
الفحوصات
[عدل]
الفحوصات تتضمن تحاليل دم وصورة أشعة للصدر وفحص وظائف الرئة وصورة طبقية عالية الجودة لمنطقة الظهر. قد يتم أخذ خزعة من الرئة إذا لم يستطع الطبيب معرفة السبب عبر السيرة المرضية أو لا يمكن إستثناء أية سرطانات.
العلاج
[عدل]المرض الرئوي الخلالي ليس مرض وحيداً بل عبارة عن مجموعة من لاأمراض ويتولد المرض بطرق عديدة، فبذلك يختلف العلاج حسب طريقة تولد المرض.
إذا كان سبب تولد المرض هو التعرض لبعض المواد المعينة (مثل إستنشاق المواد الاعضوية) فعلا المريض تجنب البيئة التي تعرضه لهذه المادة. وبنفس المبدأ، إذا كان دواء معين يسيي المرض فعليه إيقافه.
العديد من الأسباب المجهولة وأمراض النسيج الضام المسببة للمرض الرئوي العلاجي يتم علاجهم بستيرويد قشري.[22] وبعض المرضى يستجيبوا لعلاج تثبيط مناعي.
المراجع
[عدل]- ^ Disease Ontology (بالإنجليزية), 27 May 2016, QID:Q5282129
- ^ "Frequently Asked Questions About Interstitial Lung Disease - University of Chicago Medical Center".
- ^ "Interstitial Lung Disease & Pulmonary Fibrosis - UChicago Medicine". www.uchicagomedicine.org (بالإنجليزية). Retrieved 2025-01-09.
- ^ Meyer، Keith C.؛ Decker، Catherine A. (2017). "Role of pirfenidone in the management of pulmonary fibrosis". Therapeutics and Clinical Risk Management. ج. 13: 427–437. DOI:10.2147/TCRM.S81141. ISSN:1176-6336. PMC:5388201. PMID:28435277. مؤرشف من الأصل في 2024-02-25.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Bush، Andrew؛ Cunningham، Steve؛ de Blic، Jacques؛ Barbato، Angelo؛ Clement، Annick؛ Epaud، Ralph؛ Hengst، Meike؛ Kiper، Nural؛ Nicholson، Andrew G. (2015-11). "European protocols for the diagnosis and initial treatment of interstitial lung disease in children". Thorax. ج. 70 ع. 11: 1078–1084. DOI:10.1136/thoraxjnl-2015-207349. ISSN:1468-3296. PMID:26135832. مؤرشف من الأصل في 2024-08-06.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ Deterding، Robin؛ Young، Lisa R.؛ DeBoer، Emily M.؛ Warburton، David؛ Cunningham، Steven؛ Schwerk، Nicolaus؛ Flaherty، Kevin R.؛ Brown، Kevin K.؛ Dumistracel، Mihaela (2023-02). "Nintedanib in children and adolescents with fibrosing interstitial lung diseases". The European Respiratory Journal. ج. 61 ع. 2: 2201512. DOI:10.1183/13993003.01512-2022. ISSN:1399-3003. PMC:9892863. PMID:36041751. مؤرشف من الأصل في 2024-06-06.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ Maher، Toby M. (21 مايو 2024). "Interstitial Lung Disease: A Review". JAMA. ج. 331 ع. 19: 1655–1665. DOI:10.1001/jama.2024.3669. ISSN:1538-3598. PMID:38648021. مؤرشف من الأصل في 2024-06-03.
- ^ Collaborators (8 أكتوبر 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet (London, England). ج. 388 ع. 10053: 1545–1602. DOI:10.1016/S0140-6736(16)31678-6. ISSN:1474-547X. PMC:5055577. PMID:27733282. مؤرشف من الأصل في 2024-12-27.
{{استشهاد بدورية محكمة}}:|مؤلف=باسم عام (مساعدة) - ^ Bourke SJ (August 2006). "Interstitial lung disease: progress and problems". Postgrad Med J 82 (970): 494–9. doi:10.1136/pgmj.2006.046417. PMC 2585700. ببمد: 16891438.
- ^ Kreuter، Michael؛ Herth، Felix J. F.؛ Wacker، Margarethe؛ Leidl، Reiner؛ Hellmann، Andreas؛ Pfeifer، Michael؛ Behr، Jürgen؛ Witt، Sabine؛ Kauschka، Dagmar (2015). "Exploring Clinical and Epidemiological Characteristics of Interstitial Lung Diseases: Rationale, Aims, and Design of a Nationwide Prospective Registry--The EXCITING-ILD Registry". BioMed Research International. ج. 2015: 123876. DOI:10.1155/2015/123876. ISSN:2314-6141. PMC:4657073. PMID:26640781. مؤرشف من الأصل في 2023-02-17.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ "Interstitial Lung Diseases | Concise Medical Knowledge". www.lecturio.com (بالإنجليزية). Retrieved 2025-01-10.
- ^ Vehar، Susan J.؛ Yadav، Ruchi؛ Mukhopadhyay، Sanjay؛ Nathani، Avantika؛ Tolle، Leslie B. (1 فبراير 2023). "Smoking-Related Interstitial Fibrosis (SRIF) in Patients Presenting With Diffuse Parenchymal Lung Disease". American Journal of Clinical Pathology. ج. 159 ع. 2: 146–157. DOI:10.1093/ajcp/aqac144. ISSN:1943-7722. PMC:9891418. PMID:36495281. مؤرشف من الأصل في 2024-07-23.
- ^ Lee, Hyun; Choi, Hayoung; Yang, Bumhee; Lee, Sun-Kyung; Park, Tai Sun; Park, Dong Won; Moon, Ji-Yong; Kim, Tae-Hyung; Sohn, Jang Won (2 Dec 2021). "Interstitial lung disease increases susceptibility to and severity of COVID-19". European Respiratory Journal (بالإنجليزية). 58 (6). DOI:10.1183/13993003.04125-2020. ISSN:0903-1936. PMID:33888524.
- ^ Whitsett, Jeffrey A.; Wert, Susan E.; Weaver, Timothy E. (1 Feb 2010). "Alveolar Surfactant Homeostasis and the Pathogenesis of Pulmonary Disease". Annual Review of Medicine (بالإنجليزية). 61 (1): 105–119. DOI:10.1146/annurev.med.60.041807.123500. ISSN:0066-4219. Archived from the original on 2024-12-23.
- ^ "Interstitial Lung Disease A Review" (PDF). www.avancesenfibrosispulmonar.com. اطلع عليه بتاريخ 2025-01-14.
- ^ Cottin، Vincent (2016-11). "Lung biopsy in interstitial lung disease: balancing the risk of surgery and diagnostic uncertainty". The European Respiratory Journal. ج. 48 ع. 5: 1274–1277. DOI:10.1183/13993003.01633-2016. ISSN:1399-3003. PMID:27799381. مؤرشف من الأصل في 2024-12-11.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ "Interstitial Lung Diseases". The Lecturio Medical Concept Library. مؤرشف من الأصل في 2021-12-14. اطلع عليه بتاريخ 2021-07-27.
- ^ Troy، Lauren K.؛ Grainge، Christopher؛ Corte، Tamera J.؛ Williamson، Jonathan P.؛ Vallely، Michael P.؛ Cooper، Wendy A.؛ Mahar، Annabelle؛ Myers، Jeffrey L.؛ Lai، Simon (2020-02). "Diagnostic accuracy of transbronchial lung cryobiopsy for interstitial lung disease diagnosis (COLDICE): a prospective, comparative study". The Lancet. Respiratory Medicine. ج. 8 ع. 2: 171–181. DOI:10.1016/S2213-2600(19)30342-X. ISSN:2213-2619. PMID:31578168. مؤرشف من الأصل في 2024-04-24.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ "What Is Pulmonary Fibrosis?". Northwestern Medicine. مؤرشف من الأصل في 2014-02-26. اطلع عليه بتاريخ 2014-02-22.
- ^ Zare Mehrjardi M، Kahkouee S، Pourabdollah M (مارس 2017). "Radio-pathological correlation of organizing pneumonia (OP): a pictorial review". The British Journal of Radiology. ج. 90 ع. 1071: 20160723. DOI:10.1259/bjr.20160723. PMC:5601538. PMID:28106480.
- ^ ا ب Ryu JH، Olson EJ، Midthun DE، Swensen SJ (نوفمبر 2002). "Diagnostic approach to the patient with diffuse lung disease". Mayo Clinic Proceedings. ج. 77 ع. 11: 1221–7, quiz 1227. DOI:10.4065/77.11.1221. PMID:12440558.
- ^ "Interstitial lung disease: Treatments and drugs - MayoClinic.com".

