مستخدم:Ahmed Aboshama/أيض

"Metabolism". The Online Etymology Dictionary. اطلع عليه بتاريخ 2007-02-20.
Metabolism (/məˈtæbəlɪzəm/, from (باليونانية: μεταβολή) metabolē, "change") is the set of life-sustaining chemical transformations within the cells of organisms. The three main purposes of metabolism are the conversion of food/fuel to energy to run cellular processes, the conversion of food/fuel to building blocks for proteins, lipids, nucleic acids, and some carbohydrates, and the elimination of nitrogenous wastes. These enzyme-catalyzed reactions allow organisms to grow and reproduce, maintain their structures, and respond to their environments. The word metabolism can also refer to the sum of all chemical reactions that occur in living organisms, including digestion and the transport of substances into and between different cells, in which case the set of reactions within the cells is called intermediary metabolism or intermediate metabolism.
Metabolism is usually divided into two categories: catabolism, the breaking down of organic matter for example, the breaking down of glucose to pyruvate, by cellular respiration, and anabolism, the building up of components of cells such as proteins and nucleic acids. Usually, breaking down releases energy and building up consumes energy.
The chemical reactions of metabolism are organized into metabolic pathways, in which one chemical is transformed through a series of steps into another chemical, by a sequence of enzymes. Enzymes are crucial to metabolism because they allow organisms to drive desirable reactions that require energy that will not occur by themselves, by coupling them to spontaneous reactions that release energy. Enzymes act as catalysts that allow the reactions to proceed more rapidly. Enzymes also allow the regulation of metabolic pathways in response to changes in the cell's environment or to signals from other cells.
The metabolic system of a particular organism determines which substances it will find nutritious and which poisonous. For example, some prokaryotes use hydrogen sulfide as a nutrient, yet this gas is poisonous to animals.[1] The speed of metabolism, the metabolic rate, influences how much food an organism will require, and also affects how it is able to obtain that food.
A striking feature of metabolism is the similarity of the basic metabolic pathways and components between even vastly different species.[2] For example, the set of carboxylic acids that are best known as the intermediates in the citric acid cycle are present in all known organisms, being found in species as diverse as the unicellular bacterium Escherichia coli and huge multicellular organisms like elephants.[3] These striking similarities in metabolic pathways are likely due to their early appearance in evolutionary history, and their retention because of their efficacy.[4][5]
المواد الكيميائية الحيوية الرئيسية
[عدل]
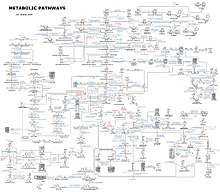
Most of the structures that make up animals, plants and microbes are made from three basic classes of molecule: amino acids, carbohydrates and lipids (often called fats). As these molecules are vital for life, metabolic reactions either focus on making these molecules during the construction of cells and tissues, or by breaking them down and using them as a source of energy, by their digestion. These biochemicals can be joined together to make polymers such as DNA and proteins, essential macromolecules of life.
Nucleotides
[عدل]The two nucleic acids, DNA and RNA, are polymers of nucleotides. Each nucleotide is composed of a phosphate attached to a ribose or deoxyribose sugar group which is attached to a nitrogenous base. Nucleic acids are critical for the storage and use of genetic information, and its interpretation through the processes of transcription and protein biosynthesis.[6] This information is protected by DNA repair mechanisms and propagated through DNA replication. Many viruses have an RNA genome, such as HIV, which uses reverse transcription to create a DNA template from its viral RNA genome.[7] RNA in ribozymes such as spliceosomes and ribosomes is similar to enzymes as it can catalyze chemical reactions. Individual nucleosides are made by attaching a nucleobase to a ribose sugar. These bases are heterocyclic rings containing nitrogen, classified as purines or pyrimidines. Nucleotides also act as coenzymes in metabolic-group-transfer reactions.[8]
"Metabolism". The Online Etymology Dictionary. اطلع عليه بتاريخ 2007-02-20.
"Metabolism". The Online Etymology Dictionary. اطلع عليه بتاريخ 2007-02-20.
Minerals and cofactors
[عدل]Inorganic elements play critical roles in metabolism; some are abundant (e.g. sodium and potassium) while others function at minute concentrations. About 99% of a mammal's mass is made up of the elements carbon, nitrogen, calcium, sodium, chlorine, potassium, hydrogen, phosphorus, oxygen and sulfur.[9] Organic compounds (proteins, lipids and carbohydrates) contain the majority of the carbon and nitrogen; most of the oxygen and hydrogen is present as water.[9]
التقويض
[عدل]Digestion
[عدل]الجزيئات الضخمة مثل النشا، أو السليولوز، أو البروتينات لا يمكن استيعابها بسرعة بواسطة الخلايا ويجب تكسيرها لوحدات أصغر قبل استخدامها في أيض الخلية. العديد من فئنات الإنزيمات المشتركة تهضم تلك البوليمرات. تلك الإنزيمات الهضمية تشمل ببتيداز الذي يهضم البروتينات إلى أحماض أمينية، بالإضافة إلى هيدروليزات الغلايكوسيد التي تهضم متعددات السكاريد إلى سكريات بسيطة تعرف باسم سكر أحادي.
تفرز الميكروبات ببساطة إنزيمات هضمية إلى البيئة المحيطة بها،[10][11] بينما تستطيع الحيوانات إفراز تلك الإنزيمات فقط من خلايا متخصصة في قناتها الهضمية التي تشمل الغدد اللعابية، والمعدة، والبنكرياس.[12] الأحماض الأمينية، أو السكريات الناتجة عن تلك الإنزيمات يتم ضخها لداخل الخلايا بواسطة بروتينات النقل النشط.[13][14]

Energy from organic compounds
[عدل]تقويض السكريات هو تكسير السكريات إلى وحدات أصغر. عادة ما يتم استيعاب السكريات لداخل الخلايا بمجرد أن يتم هضمها إلى سكريات أحادية.[15] بمجرد دخولها، الطريقة الأكبر للتحلل هي تحلل الجلوكوز، والتي يتم فيها تحويل سكريات مثل الجلوكوز والفركتوز إلى حمض البيروفيك مع توليد بعض جزيئات أدينوسين ثلاثي الفوسفات (ATP).[16] حمض البيروفيك هو مركب وسيط في العديد من المسارات الأيضية، لكن أغلبه يتم تحويله إلى أسيتيل مرافق الإنزيم-أ عن طريق تحلل الجلوكوز الهوائي ويتم تقديمه لدورة حمض السيتريك. رغم أنه يتم توليد المزيد من ATP في دورة حمض الستريك، فإن المنتج الأهم هو NADH الذي يتم تصنيعه من NAD+ عند أكسدة أسيتيل مرافق الإنزيم-أ. تحرر الأكسدة ثنائي أكسيد الكربون كمخلف للتفاعل. في الظروف اللاهوائية، يُنتج تحلل الجلوكوز حمض اللبنيك، عن طريق قيام إنزيم نازع لهيدروجين اللاكتات بإعادة أكسدة NADH إلى NAD+ ليتم استخدامه مجددا في تحلل الجلوكوز. طريق بديل لتكسير الجلوكوز هو مسار فوسفات البنتوز، الذي يختزل العامل المرافق فوسفات ثنائي نيوكليوتيد الأدينين وأميد النيكوتين NADPH وينتج سكريات خماسية مثل الريبوز.
يتم تقويض الدهون عن طريق التحلل المائي إلى أحماض دهنية حرة وغليسرول. يدخل الغليسرول في مسار تحلل الجلوكوز بينما يتم تكسير الأحماض الدهنية بواسطة أكسدة الحمض الدهني لتحرير أسيتيل مرافق الإنزيم-أ، الذي يتم تقديمه لدورة حمض الستريك. تطلق الأحماض الدهنية طاقة أكبر من السكريات عند أكسدتها لأن السكريات تحتوي على أكسجين أكثر في تركيبها. يتم تحليل الستيرويدات أيضا في بعض البكتيريا في عملية مشابهة لأكسدة الحمض الدهني، وتشمل عملية التحلل تلك إطلاق كميات كبيرة من أسيتيل مرافق الإنزيم-أ، وبروبيونيل مرافق الإنزيم-أ، وحمض البيروفيك، والذين يمكن استخدامهم جميعا بواسطة الخلية كمصدر للطاقة. بكتيريا المتفطرة السلية يمكنها أن تنمو اعتمادا على الكولسترول كمصدر وحيد للكربون، وتم التحقق من صحة أن الجينات المشاركة في مسارات استهلاك الكولسترول مهمة خلال مراحل متنوعة من دورة حياة العدوى لبكتيريا المتفطرة السلية.[17]
يتم استخدام الأحماض الأمينية إما لتصنيع البروتينات والجزيئات الحيوية الأخرى، وإما كمصدر للطاقة عن طريق أكسدتها إلى يوريا وثنائي أكسيد الكربون.[18] يبدأ مسار الأكسدة بنزع مجموعة الأمين عن طريق ناقلة الأمين. يتم تقديم مجموعة الأمين لدورة اليوريا، ما يترك هيكل كربوني منزوع الكربون في صورة حمض كيتو. العديد من أحماض الكيتو تلك تعد مركبات وسيطة في دورة حمض الستريك، على سبيل المثال نزع الأمين من حمض الجلوتاميك يكوِّن حمض ألفا كيتوجلوتاريك.[19] يمكن كذلك تحويل الأحماض الأمينية المنتجة للجلوكوز إلى جلوكوز، من خلال استحداث الجلوكوز.[20]
تحويل الطاقة
[عدل]فسفرة تأكسدية
[عدل]في الفسفرة التأكسدية، يتم إزالة الإلكترونات من الجزيئات العضوية في مناطق مثل دورة حمض البروتاغون ويتم تحويلها لأكسجين وتستخدم الطاقة المتحررة في تصنيع أدينوسين ثلاثي الفوسفات (ATP). يتم ذلك في حقيقيات النوى بواسطة سلسلة من البروتينات في أغشية الميتوكوندريا تعرف باسم سلسلة نقل الإلكترون. في بدائيات النوى، توجد تلك البروتينات في الغشاء الداخلي للخلية.[21] تستخدم تلك البروتينات الطاقة المتحررة من الالكترونات المارة عبر الجزيئات المختزلة مثل NADH لضخ البروتونات عبر الغشاء.[22]

ضخ البروتونات خارج الميتوكندريا يخلق فرق في تركيز البروتون عبر الغشاء ويولد تدرج كهروكيميائي.[23] تقود هذه القوة البروتونات مرة أخرى لداخل الميتوكندريا عن طريق قاعدة إنزيم يسمى أيه تي بي سينثاز. يجعل تدفق البروتونات الوحدة الدوارة تدور، ما يغير من شكل الموقع النشط في الإنزيم ويقوم بفسفرة ADP محولا إياه إلى ATP.
طاقة من المركبات غير العضوية
[عدل]جمادي التغذية الكيميائي هو نوع من الأيض يوجد في بدائيات النوى حيث يتم الحصول على الطاقة من أكسدة المركبات غير العضوية. يمكن لتلك المتعضيات استخدام الهيدروجين،[24] أو مركبات الكبريت المختزلة (مثل الكبريتيد، وكبريتيد الهيدروجين، وثيوكبريتات)، أو أكسيد الحديد الثنائي،[25] أو الأمونيا كمصادر لاختزال الطاقة ويحصلون على الطاقة عن طريق أكسدة تلك المركبات بواسطة قابلات الإلكترونات مثل الأكسجين أو النتريت.[26] تلك العمليات الميكروبية مهمة في الدورات الحيوية الجيولوجية الكيميائية العامة مثل تكوين الأسيتون، والنترجة، ونزع النيتروجين وهي عمليات مهمة لخصوبة التربة.[27][28]
طاقة من الضوء
[عدل]تنتزع النباتات، والبكتيريا الزرقاء، والبكتيريا الأرجوانية، والخضربيات وبعض الطلائعيات الطاقة من ضوء الشمس. ترتبط هذه العملية عادة بتحويل ثنائي أكسيد الكربون إلى مركبات عضوية، كجزء من البناء الضوئي. يمكن مع ذلك أن تتم العمليتان بشكل منفصل كما في بدائيات النوى، كما يمكن للبكتيريا الأرجوانية، والخضربيات استخدام ضوء الشمس كمصدر للطاقة مع التنقل بين تثبيت الكربون أو تخمير المواد العضوية.[29][30]
في العديد من المتعضيات يشبه انتزاع الطاقة الشمسية في المبدأ الفسفرة التأكسدية، حيث يشمل تخزين الطاقة في صورة فرق تركيز لبروتون. ذلك الفرق في التركيز هو الذي يؤدي لتصنع ATP. تأتي الإلكترونات المطلوبة لسلسة نقل الإلكترون من بروتينات جامعة للضوء تسمى رودوبسين أوثنائي نوكليوتيد الأدنين وأميد النيكوتين. يتم تقسيم مراكز رد الفعل إلى نوعين على حسب نوع صبغة البناء الضوئي الموجودة، تملك أغلب البكتيريا البانية للضوء نوع واحد، فيما تملك النباتات والبكتيريا الزرقاء نوعين.[31]
في النباتات، والطحالب، والبكتيريا الزرقاء، تستخدم وحدات النظام الثاني للبناء الضوئي الطاقة الضوئية لإزالة الإلكترونات من الماء، وتحرير الأكسجين كمخلف للتفاعل. تتدفق الإلكترونات بعد ذلك إلى سيتوكروم b6f complex، الذي يستخدم طاقتهم لضخ البروتونات عبر غشاء الثايلاكويد في البلاستيدات الخضراء. تنتقل تلك البروتونات مرة أخرى عبر الغشاء حيث تدفع أيه تي بي سينثاز -كما سبق-. تتدفق الإلكترونات بعد ذلك عبر وحدات النظام الأول للبناء الضوئي ويمكنها بعد ذلك إما أن تختزل تميم الإنزيم NADP+، لاستخدامه في دورة كالفين، أو أن يعاد تدويرها لتوليد المزيد من ATP.[32]
الابتناء
[عدل]الابتناء هو مجموعة من العمليات الأيضية البناءة يتم فيها استخدام الطاقة المتحررة من التقويض لتصنيع جزيئات معقدة. عمومًا، يتم تصنيع الجزئيات المعقدة التي تكون التركيب الخلوي خطوة بخطوة من مركبات طليعية صغيرة وبسيطة. يشمل الابتناء 3 مراحل أساسية. أولا، إنتاج المركبات الطيلعية مثل الأحماض الأمينية، والسكر الأحادي، وتربينويد، ونوكليوتيدات، وثانيا، تنشيطهم إلى صور متفاعلة باستخدام الطاقة من أدينوسين ثلاثي الفوسفات، وثالثا، تجميع تلك المركبات الطليعية لتكوين جزيئات معقدة مثل البروتينات، ومتعددات السكاريد، والدهون، والأحماض النووية.
تختلف الكائنات من حيث عدد الجزيئات التي يتم بناؤها في خلاياها. الكائنات ذاتية التغذية مثل النباتات يمكنها بناء الجزيئات العضوية المعقدة في الخلايا مثل متعددات السكاريد والبروتينات من جزيئات بسيطة مثل ثنائي أكسيد الكربون والماء. الكائنات غيرية التغذية في المقابل، تحتاج لمصدر للمواد الأكثر تعقيدا، مثل السكريات الأحادية والأحماض الأمينية، لإنتاج تلك الجزيئات المعقدة. يمكن تصنيف الكائنات بحسب المصدر النهائي للطاقة: تحصل الكائنات ضوئية التغذية، والكائنات الضوئية غيرية التغذية على الطاقة من الضوء، بينما تحصل الكائنات كيميائية التغذية، والكائنات كيميائية غيرية التغذية على الطاقة من تفاعلات أكسدة غير عضوية
تثبيت الكربون
[عدل]- ^ Friedrich C (1998). "Physiology and genetics of sulfur-oxidizing bacteria". Adv Microb Physiol. Advances in Microbial Physiology. ج. 39: 235–89. DOI:10.1016/S0065-2911(08)60018-1. ISBN:978-0-12-027739-1. PMID:9328649.
- ^ Pace NR (يناير 2001). "The universal nature of biochemistry". Proc. Natl. Acad. Sci. U.S.A. ج. 98 ع. 3: 805–8. Bibcode:2001PNAS...98..805P. DOI:10.1073/pnas.98.3.805. PMC:33372. PMID:11158550.
- ^ Smith E، Morowitz H (2004). "Universality in intermediary metabolism". Proc Natl Acad Sci USA. ج. 101 ع. 36: 13168–73. Bibcode:2004PNAS..10113168S. DOI:10.1073/pnas.0404922101. PMC:516543. PMID:15340153.
- ^ Ebenhöh O، Heinrich R (2001). "Evolutionary optimization of metabolic pathways. Theoretical reconstruction of the stoichiometry of ATP and NADH producing systems". Bull Math Biol. ج. 63 ع. 1: 21–55. DOI:10.1006/bulm.2000.0197. PMID:11146883.
- ^ Meléndez-Hevia E، Waddell T، Cascante M (1996). "The puzzle of the Krebs citric acid cycle: assembling the pieces of chemically feasible reactions, and opportunism in the design of metabolic pathways during evolution". J Mol Evol. ج. 43 ع. 3: 293–303. Bibcode:1996JMolE..43..293M. DOI:10.1007/BF02338838. PMID:8703096.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعNelson - ^ Sierra S، Kupfer B، Kaiser R (2005). "Basics of the virology of HIV-1 and its replication". J Clin Virol. ج. 34 ع. 4: 233–44. DOI:10.1016/j.jcv.2005.09.004. PMID:16198625.
- ^ Wimmer M، Rose I (1978). "Mechanisms of enzyme-catalyzed group transfer reactions". Annu Rev Biochem. ج. 47: 1031–78. DOI:10.1146/annurev.bi.47.070178.005123. PMID:354490.
- ^ ا ب Heymsfield S، Waki M، Kehayias J، Lichtman S، Dilmanian F، Kamen Y، Wang J، Pierson R (1991). "Chemical and elemental analysis of humans in vivo using improved body composition models". Am J Physiol. ج. 261 ع. 2 Pt 1: E190–8. PMID:1872381.
- ^ "Bacterial extracellular zinc-containing metalloproteases". Microbiol Rev. ج. 57 ع. 4: 823–37. December 1993. DOI:10.1074/jbc.R600011200. PMID:8302217.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|year=لا يطابق|date=(مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link)تحقق من التاريخ في:|year= / |date= mismatch(مساعدة) - ^ "Bacterial lipases: an overview of production, purification and biochemical properties". Appl Microbiol Biotechnol. ج. 64 ع. 6: 763–81. 2004. DOI:10.1007/s00253-004-1568-8. PMID:14966663.
- ^ Hoyle T (1997). "The digestive system: linking theory and practice". Br J Nurs. ج. 6 ع. 22: 1285–91. PMID:9470654.
- ^ "How amino acids get into cells: mechanisms, models, menus, and mediators". JPEN J Parenter Enteral Nutr. ج. 16 ع. 6: 569–78. 1992. DOI:10.1177/0148607192016006569. PMID:1494216.
- ^ "Structure and function of facilitative sugar transporters". Curr Opin Cell Biol. ج. 11 ع. 4: 496–502. 1999. DOI:10.1016/S0955-0674(99)80072-6. PMID:10449337.
- ^ "Structure and function of mammalian facilitative sugar transporters". J Biol Chem. ج. 268 ع. 26: 19161–4. 1993. PMID:8366068.
- ^ "The cellular fate of glucose and its relevance in type 2 diabetes". Endocr Rev. ج. 25 ع. 5: 807–30. 2004. DOI:10.1210/er.2003-0026. PMID:15466941.
- ^ Wipperman، Matthew, F.؛ Thomas، Suzanne, T.؛ Sampson، Nicole, S. (2014). "Pathogen roid rage: Cholesterol utilization by Mycobacterium tuberculosis". Crit. Rev. Biochem. Mol. Biol. ج. 49 ع. 4: 269–93. DOI:10.3109/10409238.2014.895700. PMID:24611808.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Amino acid metabolism". Annu Rev Biochem. ج. 32: 355–98. 1963. DOI:10.1146/annurev.bi.32.070163.002035. PMID:14144484.
- ^ Brosnan J (2000). "Glutamate, at the interface between amino acid and carbohydrate metabolism". J Nutr. ج. 130 ع. 4S Suppl: 988S–90S. PMID:10736367.
- ^ "Glutamine: the emperor or his clothes?". J Nutr. ج. 131 ع. 9 Suppl: 2449S–59S, discussion 2486S–7S. 2001. PMID:11533293.
- ^ "Energy Transduction: Proton Transfer Through the Respiratory Complexes". Annu Rev Biochem. ج. 75: 165–87. 2006. DOI:10.1146/annurev.biochem.75.062003.101730. PMID:16756489.
- ^ "Structures and proton-pumping strategies of mitochondrial respiratory enzymes". Annu Rev Biophys Biomol Struct. ج. 30: 23–65. 2001. DOI:10.1146/annurev.biophys.30.1.23. PMID:11340051.
- ^ "Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor". Trends Biochem Sci. ج. 27 ع. 3: 154–60. 2002. DOI:10.1016/S0968-0004(01)02051-5. PMID:11893513.
- ^ "Molecular biology of hydrogen utilization in aerobic chemolithotrophs". Annu Rev Microbiol. ج. 47: 351–83. 1993. DOI:10.1146/annurev.mi.47.100193.002031. PMID:8257102.
- ^ "Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction". Nat Rev Microbiol. ج. 4 ع. 10: 752–64. 2006. DOI:10.1038/nrmicro1490. PMID:16980937.
- ^ Simon J (2002). "Enzymology and bioenergetics of respiratory nitrite ammonification". FEMS Microbiol Rev. ج. 26 ع. 3: 285–309. DOI:10.1111/j.1574-6976.2002.tb00616.x. PMID:12165429.
- ^ Conrad R (1996). "Soil microorganisms as controllers of atmospheric trace gases (H2, CO, CH4, OCS, N2O, and NO)". Microbiol Rev. ج. 60 ع. 4: 609–40. PMID:8987358.
- ^ "Microbial co-operation in the rhizosphere". J Exp Bot. ج. 56 ع. 417: 1761–78. 2005. DOI:10.1093/jxb/eri197. PMID:15911555.
- ^ "Diel Variations in Carbon Metabolism by Green Nonsulfur-Like Bacteria in Alkaline Siliceous Hot Spring Microbial Mats from Yellowstone National Park". Appl Environ Microbiol. ج. 71 ع. 7: 3978–86. يوليو 2005. DOI:10.1128/AEM.71.7.3978-3986.2005. PMID:16000812.
- ^ "Interactive Control of Rhodobacter capsulatus Redox-Balancing Systems during Phototrophic Metabolism". J Bacteriol. ج. 183 ع. 21: 6344–54. 2001. DOI:10.1128/JB.183.21.6344-6354.2001. PMID:11591679.
- ^ "Photosynthetic reaction centers". FEBS Lett. ج. 438 ع. 1–2: 5–9. 1998. DOI:10.1016/S0014-5793(98)01245-9. PMID:9821949.
- ^ "Cyclic electron flow around photosystem I is essential for photosynthesis". Nature. ج. 429 ع. 6991: 579–82. 2004. Bibcode:2004Natur.429..579M. DOI:10.1038/nature02598. PMID:15175756.

البناء الضوئي هو تصنيع الكربوهيدرات من ضوء الشمس وثنائي أكسيد الكربون. في النبات، والبكتيريا الزرقاء، والطحالب، البناء الضوئي الأكسجيني يقسم الماء، وينتج الأكسجين كمخلفات للتفاعل. تستخدم هذه العملية أدينوسين ثلاثي الفوسفات (ATP) وثنائي نوكليوتيد الأدنين وأميد النيكوتين (NADPH) الناتجان عن مراكز رد فعل البناء الضوئي لتحويل ثنائي أكسيد الكربون إلى حمض 3-فوسفوغليسيريك، الذي يمكن تحويله بعد ذلك إلى جلوكوز. يتم تنفيذ تفاعل تثبيت الكربون بواسطة إنزيم روبيسكو كجزء من دورة كالفين.[1] يحدث 3 أنواع من البناء الضوئي في النباتات: تمثيل ضوئي ثلاثي الكربون، وتمثيل ضوئي رباعي الكربون، وأيض حامض المخلدات. الفرق بين أولئك هو الطريق الذي يسلكه ثنائي أكسيد الكربون نحو دورة كالفين، ففي ثلاثي الكربون يقوم النبات بتثبيت ثنائي أكسيد الكربون مباشرة، أما في النوعين الآخرين يدمج البناء الضوئي ثنائي أكسيد الكربون في المركبات الأخرى أولا، كطريقة للتكيف مع ضوء الشمس القوي والظروف الجافة.[2]
في بدائيات النوى التي تقوم بالبناء الضوئي، آليات تثبيت الكربون أكثر تنوعا. حيث يمكن تثبيت ثنائي أكسيد الكربون بواسطة دورة كالفين، وهي دورة حمض الستريك ولكن معكوسة،[3] أو عن طريق إضافة كربوكسيل لأسيتيل مرافق الإنزيم-أ.[4][5] بدائيات النوى كيميائية التغذية تثبت ثنائي أكسيد الكربون عبر دورة كالفين، ولكنها تستخدم الطاقة الصادرة من المركبات غير العضوية لتحفيز التفاعل.[6]
السكريات والغليكانات
[عدل]في ابتناء السكريات، يمكن تحويل الأحماض العضوية البسيطة إلى سكريات أحادية مثل الجلوكوز ثم تجميعها لتكوين متعددات السكاريد مثل النشا. توليد الجلوكوز من مركبات مثل حمض البيروفيك، وحمض اللبنيك، وغليسرول، وحمض 3-فوسفوغليسيريك، والأحماض الأمينية يسمى استحداث الجلوكوز. يحول استحداث الجلوكوز حمض البيروفيك إلى جلوكوز 6-فوسفات عبر سلسلة من المركبات الوسطية، تشترك العديد منها في تحلل الجلوكوز. على أي حال، هذا المسار ليس مجرد تحلل الجلوكوز بشكل معكوس، حيث أن العديد من الخطوات يتم تحفيزها بإنزيمات غير موجودة في تحلل الجلوكوز. هذا الأمر مهم حيث يسمح بتنظيم تكوين وتكسير الجلوكوز بشكل منفصل، ويمنع حدوث المسارين بالتزامن في حلقة مفرغة.[7][8]
رغم أن الدهون هي طريقة شائعة لتخزين الطاقة، في الفقاريات مثل الإنسان لا يمكن تحويل الأحماض الدهنية في تلك المخازن إلى جلوكوز من خلال استحداث الجلوكوز حيث أن تلك الكائنات لا يمكنها تحويل أسيتيل مرافق الإنزيم-أ إلى حمض البيروفيك، تمتلك النباتات الإنزيمات الضرورية لذلك بينما لا تمتلكها الحيوانات.[9] نتيجة لذلك، بعد فترة طويلة من المجاعة، تحتاج الفقاريات لإنتاج أجسام كيتونية من الأحماض الدهنية لاستبدال الجلوكوز في الأنسجة مثل المخ الذي لا يستطيع أيض الأحماض الدهنية.[10] في الكائنات الأخرى كالنباتات والبكتيريا، يتم حل تلك المشكلة الأيضية باستخدام دورة الجلايكسولات، التي تتجاوز خطوة نزع الكربوكسيل الموجودة في دورة حمض الستريك وتسمح بتحول أسيتيل مرافق الإنزيم-أ إلى حمض أكسالوأسيتيك، الذي يمكن استخدامه لإنتاج الجلوكوز.[9][11]
يتم تصنيع متعددات السكاريد والغليكانات عن طريق إضافة متتابعة للسكريات الأحادية بواسطة إنزيم ناقل الغليكوزيل من سكر-فوسفات تفاعلي متبرع مثل غلوكوز ثنائي فوسفات اليوريدين إلى مجموعة هيدروكسيل مستقبلة على متعدد السكاريد النامي. نظرًا لأن أي من مجموعات الهيدروكسيل على حلقة المادة المتفاعلة يمكن أن تكون مستقبلة، يمكن أن يكون متعدد السكاريد الناتج إما متفرع أو مستقيم.[12] يمكن أن تمتلك متعددات السكاريد الناتجة وظائف تركيبية أو أيضية، أو يتم تحويلها إلى دهون أو بروتينات.[13][14]
الأحماض الدهنية، وتربينويد، وستيرويدات
[عدل]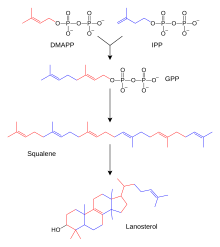
يتم تصنيع الأحماض الدهنية بواسطة إنزيم مصنع الحمض الدهني الذي يبلمر ثم يختزل وحدات أسيتيل مرافق الإنزيم-أ. حلقات الأسيل الموجودة في الأحماض الدهنية تتمدد بواسطة حلقة من التفاعلات التي تضيف مجموعة الأسيل، وتختزلها إلى كحول، ثم تنزع منها الماء لتحولها إلى مجموعة ألكين ثم تختزلها مجددا إلى مجموعة ألكان. تنقسم إنزيمات التصنيع الحيوي للأحماض الدهنية إلى مجموعتين: في الحيوانات والفطريات، يتم تنفيد كل تفاعلات تصنيع الحمض الدهني بواسطة بروتين واحد متعدد الوظائف،[15] أما في بلاستيدات النبات وفي البكتيريا يؤدي إنزيم مختلف كل خطوة في المسار.[16][17]
تربين، وتربينويد هما فئة كبيرة من الدهون التي تشمل كاروتينات وتشكل الفئة الأكبر من المنتجات الطبيعية للنبات.[18] يتم تصنيع تلك المركبات عن طريق تجميع وتعديل وحدات إيزوبرين التي تتبرع بها مركبات طليعية متفاعلة.[19] تفاعل مهم يستخدم المركبات المتبرعة بإيزوبرين هو تصنيع الستيرويد. حيث تنضم وحدات إيزوبرين لبعضها لبعض لتكوين سكوالين ثم يتم طيها لتشكيل مجموعة من الحلقات لتكون لانوستيرول.[20] يمكن بعد ذلك تحويل لانوستيرول ‘لى ستيرويدات أخرى مثل كولسترول وإرغوستيرول.[21]
البروتينات
[عدل]تختلف الكائنات في قدرتها على تصنيع الـ20 حمض أميني المشتركة. تستطيع أغلب البكتيريا والنباتات تصنيع العشرين حمض جميعهم، إلا أن الثدييات تستطيع تصنيع 11 حمض أميني غير ضروري، لذلك فإن 9 أحماض أمينية ضرورية يجب الحصول عليها من الغذاء. بعض الطفيليات البسيطة، مثل بكتيريا المفطورة الرئوية، تفتقد القدرة على تصنيع أي من الأحماض الأمينية وتحصل على أحماضها الأمينية مباشرة من العائل.[22] يتم تصنيع كل الأحماض الأمينية من مركبات وسطية في تحلل الجلوكوز، ودورة حمض الستريك، أو مسار فوسفات البنتوز. يتم توفير النيتروجين بواسطة حمض الجلوتاميك والجلوتامين. يعتمد تصنيع الأحماض الأمينية على تكوين حمض كيتو ألفا المناسب، الذي يتم نقل مجموعة الأمين له لتكوين حمض أميني.[23]
يتم تصنيع البروتينات من الأحماض الأمينية عن طريق ضم بعضها لبعض في سلسلة من الروابط الببتيدية. يملك كل بروتين مختلف تسلسل فريد من الأحماض الأمينية: وهذا هو تركيبه الأولي. تماما كما يمكن دمج حروف الأبجدية لتكوين عدد لا نهائي من الكلمات، يمكن ربط الأحماض الأمينية في تسلسلات مختلفة لتكوين عدد هائل من البروتينات. يتم تصنيع البروتينات من الأحماض الأمينية التي تم تنشيطها عن طريق الارتباط بجزئ حمض نووي ريبوزي ناقل برابطة إستر. يتم إنتاج هذا المركب الطليعي في تفاعل يعتمد على أدينوسين ثلاثي الفوسفات.[24] يعد هذا المركب ركيزة للريبوسوم، الذي ينضم إلى الحمض الأميني على سلسلة البروتين المطوي ، باستخدام معلومات التسلسل في الحمض النووي الريبوزي الرسول.[25]
تصنيع وإنقاذ النوكليوتيد
[عدل]تتكون النوكليوتيدات من أحماض أمينية، وثنائي أكسيد الكربون، وحمض الفورميك في مسارات تتطلب كميات كبيرة من الطاقة الأيضية.[26] بناء على ذلك، تمتلك أغلب الكائنات أنظمة فعالة لإنقاذ النوكليوتيدات المتكونة.[27] يتم تصنيع البيورين كنيوكليوسيد (قواعد مرتبطة بالريبوز).[28] كل من الأدينين، والغوانين يتم تصنيعهما من مركب نيوكلوسيد طليعي إينوسين أحادي الفوسفات، الذي يتم تصنيعه باستخدام ذرات من الأحماض الأمينية جلايسين، وجلوتامين، وحمض الأسبارتيك. في المقابل، يتم تصنيع بيريميدين من أوروتيت، الذي يتم تصنيعه من جلوتامين وحمض الأسبارتيك.[29]
الدخيل الحيوي وأيض الأكسدة والاختزال
[عدل]تتعرض كل الكائنات الحية باستمرار إلى مركبات لا يمكنهم استخدامها كغذاء وتكون ضارة إذا تراكمت في الخلايا، حيث لا توجد وظيفة أيضية له. تلك المركبات التي يحتمل أن تكون ضارة تسمى الغريب الحيوي أو الدخيل الحيوي.[30] الدخائل الحيوي مثل الأدوية المصنعة، والسموم الطبيعية، والمضادات الحيوية يتم إزالة سميتها بمجموعة من الإنزيمات الأيضية للغريب الحيوي. في الإنسان، تشمل تلك الإنزيمات مؤكسدات سيتوكروم بي450،[31] وغلوكويورنوسايل ترانسفيراز،,[32] وجلوتاثيون أس-ترانسفيراز.[33] يعمل هذا الجهاز من الإنزيمات في 3 مراحل لأكسدة الغريب الحيوي أولاً (المرحلة 1) ثم ربط مجموعات قابلة للذوبان في الماء للجزئ (المرحلة 2). الغريب الحيوي المعدل القابل للذوبان في الماء يمكن بعد ذلك ضخة خارج الخلايا وفي الكائنات متعددة الخلايا يمكن أيضه أكثر من ذلك قبل إخراجه (المرحلة 3). في علم البيئة، تلك التفاعلات مهمة بالأخص في التحلل الحيوي الميكروبي للملوثات والمعالجة الحيوية للأرض الملوثة وتسرب النفط.[34] العديد من تلك التفاعلات الميكروبية تتواجد في كائنات متعددة الخلايا، ولكن بسبب التنوع الكبير في أنواع الميكروبات فإن تلك الكائنات قدرة على التعامل مع نطاق أوسع بكثير من الدخائل الحيوية مقارنة بالكائنات متعددة الخلايا، ويمكنها حتى تحليل الملوثات العضوية الثابتة مثل مركبات الكلوريد العضوي.[35]
مشكلة متعلقة بالكائنات الهوائية هي الإجهاد التأكسدي.[36] هنا، العمليات التي تشمل فسفرة تأكسدية وتكوين روابط ثنائية الكبريتيد خلال تطوي البروتين تنتج أنواع الأكسجين التفاعلية مثل بيروكسيد الهيدروجين.[37] تلك المؤكسدات الضارة تتم إزالتها بواسطة مستقلبات مضادة للتأكسد مثل جلوتاثيون وإنزيمات مثل كاتالاز وبيروكسيداز.[38][39]
Thermodynamics of living organisms
[عدل]Living organisms must obey the laws of thermodynamics, which describe the transfer of heat and work. The second law of thermodynamics states that in any closed system, the amount of entropy (disorder) cannot decrease. Although living organisms' amazing complexity appears to contradict this law, life is possible as all organisms are open systems that exchange matter and energy with their surroundings. Thus living systems are not in equilibrium, but instead are dissipative systems that maintain their state of high complexity by causing a larger increase in the entropy of their environments.[40] The metabolism of a cell achieves this by coupling the spontaneous processes of catabolism to the non-spontaneous processes of anabolism. In thermodynamic terms, metabolism maintains order by creating disorder.[41]
التنظيم والتحكم
[عدل]نظرًا لأن بيئة أغلب الكائنات تتغير باستمرار، يجب أن يتم تنظيم تفاعلات الأيض بشكل دقيق للحفاظ على مجموعة ثابتة من الظروف داخل الخلايا، فيما يعرف باسم الاستتباب.[42][43] يسمح تنظيم الأيض كذلك للكائنات الحية بالاستجابة للإشارات والتفاعل بشكل نشط مع بيئاتهم.[44] مبدآن مترابطان بشكل كبير مهمان للغاية في فهم كيفية التحكم في المسارات الأيضية. الأول، أن تنظيم إنزيم ما في مسار ما هو كيف أن نشاطه يزيد ويقل استجابة لإشارات. الثاني، أن التحكم الذي يبذله ذلك الإنزيم هو تأثير تلك التغيرات في نشاطه على المعدل الكلي للمسار.[45] على سبيل المثال، قد يُظهر إنزيم ما تغيرات كبيرة في نشاطه (أي أنه منظم بشكل كبير) لكن إذا كانت تلك التغيرات لها أثر بسيط على معدل المسار الأيضي، فإن هذا الإنزيم ليس مساهما في التحكم في ذلك المسار.[46]

توجد العديد من مستويات تنظيم الأيض. في التنظيم الداخلي، يقوم المسار الأيضي بتنظيم نفسه ليستجيب للتغيرات في مستويات الركائز أو المنتجات، على سبيل المثال، نقص كمية المادة المنتجة يزيد التدفق عبر المسار من أجل التعويض. يتضمن هذا النوع من التنظيم عادة تنظيم تفارغي لنشاطات العديد من الإنزيمات في المسار.[47] يتضمن التحكم الخارجي في كائن متعدد الخلايا أن تقوم خلية بتعيير أيضها استجابة لإشارات من خلايا أخرى. تلك الإشارات عادة تكون في صورة رسل ذائبة مثل الهرمونات وعوامل النمو ويتم اكتشفها بواسطة مستقبلات على سطح الخلية.[48] يتم بعد ذلك بث تلك الإشارات داخل الخلية بواسطة أنظمة الرسول الثاني التي تشارك غالبا في فسفرة البروتينات.[49]
نموذج مفهوم جدا للتحكم الخارجي هو تنظيم أيض الجلوكوز بواسطة هرمون الإنسولين.[50] يتم إنتاج الإنسولين استجابة لارتفاع سكر الدم. ارتباط الهرمون بمستقبلة الإنسولين على الخلايا ينشط سلسة من البروتين كيناز التي تؤدي لاستيعاب الخلايا للجلوكوز من الدم وتحويله إلى جزيئات تخزين مثل الأحماض الدهنية والغلايكوجين.[51] يتم التحكم في أيض الغلايكوجين عبر نشاط إنزيم فوسفوريلاز، وهو الإنزيم الذي يكسر الغلايكوجين، و غلايكوجين سينثاز، الإنزيم الذي يصنعه. يتم تنظيم تلك الإنزيمات بشكل متبادل، حيث تثبط الفسفرة غلايكوجين سينثاز، وتنشط فوسفوريلاز. يتسبب الإنسولين في تصنيع الغلايكوجين عن طريق تنشيط فوسفاتاز البروتين والتسبب في نقص فسفرة تلك الإنزيمات.[52]
التطور
[عدل]
المسارات المركزية للأيض المذكورة سابقًا، مثل تحلل الجلوكوز، ودورة حمض الستريك، تتواجد في النطاقات الثلاثة للكائنات الحية وكانت متواجدة كذلك في السلف الشامل الأخير.[53][54] كانت خلية السلف الشامل بدائية النوى ومولدة للميثان غالبا وبها الكثير من أيض الحمض الأميني، والنوكوليوتيد، والسكريات، والدهون..[55][56] قد يكون الإبقاء على هذه المسارات القديمة خلال التطور المتأخر ناتجا عن أن هذه التفاعلات كانت الحل الأمثل لمشاكلهم الأيضية الخاصة، مع مسارات مثل تحلل الجلوكوز ودورة حمض الستريك تنتج نواتجها النهائية بفعالية عالية وبعدد محدود من الخطوات.[57][58] قد تكون المسارات الأولى في الأيض القائم على الإنزيمات جزءًا من أيض نوكليوتيد البيورين، فيما كانت مسارات الأيض السابقة جزءًا من فرضية عالم الحمض النووي الريبوزي القديمة.[59]
تم اقتراح العديد من النماذج لوصف آليات تطور مسارات الأيض الحديثة. تشمل تلك النماذج إضافات متتابعة لإنزيمات جديدة لمسارات قديمة قصيرة، وتضاعف ثم تشعب المسارات بالكامل بالإضافة لتوظيف الانزيمات الموجودة مسبقا وتجميعها في مسار تفاعل جديد.[60] الأهمية النسبية لتلك الآليات غير واضحة، إلا أن دراسات جينومية أظهرت أن الإنزيمات في مسار ما من المحتمل أن يكون لها سلف مشترك، ما يقترح أن العديد من المسارات قد تطورت خطوة بخطوة مع تكوُّن وظائف جديدة من الخطوات الموجودة سابقًا في المسار.[61] نموذج بديل ظهر من دراسات تتبع تطور تركيب البروتيان في شبكة الأيض، اقترح ذلك النموذج أن الإنزيمات يتم توظيفها بشكل واسع، واستعارة إنزيمات لتأدية وظائف مشابهة في مسارات أيضية مختلفة.[62] تؤدي عملية التوظيف تلك إلى تنوع في التطور الإنزيمي.[63] احتمال ثالث هو أن بعض أجزاء الأيض قد تتواجد في "وحدات" يمكن إعادة استخدماها في مسارات مختلفة وتؤدي نفس الوظائف على جزيئات مختلفة.[64]
بالإضافة لتطور مسارات أيضية جديدة، يمكن أن يسبب التطور كذلك فقد بعض الوظائف الأيضية. على سبيل المثال، في بعض الديدان فُقدت العمليات الأيضية غير الضرورية للحياة، وعوضًا عنها يمكن استغلال الأحماض الأمينية، والنوكليوتيدات، والسكريات الموجودة مسبقًا في العائل.[65] يمكن ملاحظة أمثلة مشابهة لفقد القدرات الأيضية في كائنات المعايشة الجوانية.[66]
الاستقصاء والمعالجة
[عدل]
بشكل تقليدي، تتم دراسة الأيض بمقاربة اختزالية تركز على مسار أيضي واحد. استعمال القائفات المشعة مفيد بشكل خاص في تعقب الكائن بالكامل، وعلى مستوى النسيج، والخلية، والذي يحدد المسار من المركب الطليعي حتى الناتج النهائي عن طريق التعرف على الوسائط والمنتجات المعلمة بمادة مشعة.[67] الإنزيمات التي تحفز تلك التفاعلات الكيميائية يمكن بعد ذلك تنقيتها ودراسة حركياتها واستجابتها للمثبطات. مقاربة موازية هي التعرف على الجزئيات الصغيرة في خلية أو نسيج، المجموعة الكاملة من تلك الجزيئات تسمى ميتابولوم. بشكل عام، تعطي تلك الدراسات نظرة جيدة على تركيب ووظيفة المسارات الأيضية البسيطة، لكنها غير كافية عند تطبيقها على أنظمة أكثر تعقيدا مثل أيض خلية كاملة.[68]
يمكن الحصول على فكرة عن مدى تعقيد شبكات الأيض في الخلايا التي تحتوي على آلاف الإنزيمات المختلفة عن طريق الشكل الموضح في الصورة الذي يعرض التفاعلات بين 43 بروتينًا و40 مستقلبًا فقط: توفر تسلسلات الجينومات قوائم تحتوي على ما يصل إلى 45,000 جين.[69] مع ذلك، من الممكن الآن استخدام تلك البيانات الجينومية لإعادة تشكيل شبكات كاملة من التفاعلات الكيميائية الحيوية وإنتاج نماذج رياضية أكثر كلية قد تشرح وتتوقع سلوكياتهم.[70] تلك النماذج قوية بشكل خاص حين تستخدم لدمج بيانات المسار والمستقلب المحصول عليها عبر الطرق التقليدية مثل التعبير الجيني من الدراسات البروتيومية ومصفوفة دي إن إيه الدقيقة.[71] باستخدام تلك الطرق، تم انتاج نموذج لأيض الإنسان، ما سيساعد فى اكتشاف أدوية مستقبلية وأبحاث الكيمياء الحيوية.[72] تستخدم تلك النماذج الآن في تحليل الشبكات، لتصنيف أمراض الإنسان في مجموعات تتشارك في بروتينات أو مستقلبات مشتركة.[73][74]
تعد شبكات الأيض البكتيرية مثالا صارخًا على تنظيم ربطة العنق على شكل قوس،[75][76] وهو تركيب قادر على إدخال نطاق واسع من المغذيات وإنتاج مجموعة كبيرة من المنتجات والجزيئات الكبيرة المعقدة باستخدام تداولات وسيطة مشتركة قليلة نسبيًا.
تطبيق تكنولوجي كبير لتلك المعلومات هو الهندسة الأيضية. وفيها يتم تعديل بعض الكائنات كالخميرة، أو النباتات، أو البكتيريا جينيًا لجعلهم أكثر فائدة في التكنولوجيا الحيوية وللمساعدة في إنتاج أدوية مثل المضادات الحيوية أو الكيماويات الصناعية مثل حمض الشيكيميك.[77] تهدف تلك التعديلات الجينية عادة لتقليل كم الطاقة المستخدم لإنتاج المنتج، وزيادة الإنتاجية، وتقليل مخلفات الإنتاج.[78]
التاريخ
[عدل]
يحتوي كتاب أجزاء الحيوان لأرسطو على تفاصيل كافية عن وجهة نظره بشأن الأيض تكفي لصنع نموذج تدفق مفتوح. حيث آمن أن كل مرحلة من العملية، يتم فيها تحويل مواد من الطعام، مع إطلاق حرارة بإعتباره العنصر التقليدي للحريق، وفضلات يتم إخراجها في صورة بول، أو براز، أو صفراء.[79]
وصف ابن النفيس الأيض في عام 1260 في روايته الرسالة الكاملية في السيرة النبوية والتي احتوت عبارة "كل من الجسم وأجزاءه في حالة مستمرة من الانحلال والبناء، لذلك هي حتما تمر بتغيير دائم."[80] يمتد تاريخ الدراسة العلمية للتمثيل الغذائي لعدة قرون وانتقل من دراسة الحيوانات بالكامل في الدراسات المبكرة، لدراسة التفاعلات الأيضية المفردة في الكيمياء الحيوية الحديثة. تم نشر التجارب المخططة الأولى لأيض الإنسان في 1614 بواسطة سانتوريو سانتوري في كتابه حرق الطب الساكن.[81] وصف فيه كيف وزن نفسه قبل وبعد الأكل، والنوم، والعمل، وممارسة الجنس، والصوم، والشرب، والإخراج. حيث وجد أن أغلب الطعام الذي تناوله قد فقد عبر ما أسماه "عرق غير ملموس".

في تلك الدراسات المبكرة، لم يتم التعرف على آليات تلك العمليات الأيضية وكان من المعتقد أن هناك قوة حيوية تنشط الأنسجة الحية.[82] في القرن الـ19، عند دراسة تخمير السكر إلى كحول بواسطة الخميرة، استنتج لويس باستور أن التخمير تم تحفيزه بواسطة مواد في خلايا الخميرة أسماها "مخمرات". كتب أن "التخمير الكحولي هو عمل مرتبط بحياة وتنظيم خلايا الخميرة، وليس مع موت أو تعفن الخلايا."[83] هذا الاكتشاف، إلى جانب ما نشره فريدرش فولر في 1828 عن بحث حول التصنيع الكيميائي لليوريا،[84] وكونها أول مركب عضوي يحضر بالكامل من مركبات طليعية غير عضوية أثبتا أن المركبات العضوية والتفاعلات الكيميائية الموجودة في الخلية لا تختلف من حيث المبدأ عن أي جزء من الكيمياء.
كان اكتشاف الإنزيمات في بدايات القرن الـ20 بواسطة إدوارد بوخنر هو ما فصل دراسة تفاعلات الأيض الكيميائية عن الدراسة البيولوجية للخلايا، وأشار ببدء الكيمياء الحيوية.[85] نما حجم المعرفة الكيميائية الحيوية بسرعة خلال أوائل القرن الـ20. أحد أكثر علماء الكيمياء الحيوية الجدد المثمرين وقتها كان هانس كريبس الذي قدم إسهامات هائلة في دراسة الأيض.[86] اكتشف كريبس دورة اليوريا ولاحقًا، بالتعاون مع هانز كورنبيرج، دورة حمض الستريك ودورة الجلايكسولات.[87] تمت مساعدة أبحاث الكيمياء الحيوية الحديثة بشكل كبير بسبب تطور التقنيات الحديثة مثل الاستشراب، ودراسة البلورات بالأشعة السينية، ومطيافية الرنين المغناطيسي النووي، والوسم النظيري، والمجهر الإلكتروني. سمحت تلك التقنيات باكتشاف والتحليل المفصل للعديد من الجزيئات والمسارات الأيضية في الخلايا.
انظر أيضا
[عدل]- مضاد المئيضة
- معدل الأيض الأساسي
- مسعرية
- خطأ أيضي خلقي
- فرضية عالم الحديد والكبريت، نظرية "الأيض أولًا" عن منشأ الحياة
- اضطراب أيضي
- مجموعات غذائية أساسية
- أيض جرياني
- أيض الكبريت
- أيض فيضي
- موسوعة كيوتو للجينات والمجينات
مراجع
[عدل]- ^ Bouché C، Serdy S، Kahn C، Goldfine A (2004). "The cellular fate of glucose and its relevance in type 2 diabetes". Endocr Rev. ج. 25 ع. 5: 807–30. DOI:10.1210/er.2003-0026. PMID:15466941.
- ^ Dodd A، Borland A، Haslam R، Griffiths H، Maxwell K (2002). "Crassulacean acid metabolism: plastic, fantastic". J Exp Bot. ج. 53 ع. 369: 569–80. DOI:10.1093/jexbot/53.369.569. PMID:11886877.
- ^ Sakami W، Harrington H (1963). "Amino acid metabolism". Annu Rev Biochem. ج. 32: 355–98. DOI:10.1146/annurev.bi.32.070163.002035. PMID:14144484.
- ^ Brosnan J (2000). "Glutamate, at the interface between amino acid and carbohydrate metabolism". J Nutr. ج. 130 ع. 4S Suppl: 988S–90S. PMID:10736367.
- ^ Young V، Ajami A (2001). "Glutamine: the emperor or his clothes?". J Nutr. ج. 131 ع. 9 Suppl: 2449S–59S, discussion 2486S–7S. PMID:11533293.
- ^ Shively J، van Keulen G، Meijer W (1998). "Something from almost nothing: carbon dioxide fixation in chemoautotrophs". Annu Rev Microbiol. ج. 52: 191–230. DOI:10.1146/annurev.micro.52.1.191. PMID:9891798.
- ^ Hosler J، Ferguson-Miller S، Mills D (2006). "Energy Transduction: Proton Transfer Through the Respiratory Complexes". Annu Rev Biochem. ج. 75: 165–87. DOI:10.1146/annurev.biochem.75.062003.101730. PMC:2659341. PMID:16756489.
- ^ Schultz B، Chan S (2001). "Structures and proton-pumping strategies of mitochondrial respiratory enzymes". Annu Rev Biophys Biomol Struct. ج. 30: 23–65. DOI:10.1146/annurev.biophys.30.1.23. PMID:11340051.
- ^ ا ب Ensign S (2006). "Revisiting the glyoxylate cycle: alternate pathways for microbial acetate assimilation". Mol Microbiol. ج. 61 ع. 2: 274–6. DOI:10.1111/j.1365-2958.2006.05247.x. PMID:16856935.
- ^ Finn P، Dice J (2006). "Proteolytic and lipolytic responses to starvation". Nutrition. ج. 22 ع. 7–8: 830–44. DOI:10.1016/j.nut.2006.04.008. PMID:16815497.
- ^ Kornberg H، Krebs H (1957). "Synthesis of cell constituents from C2-units by a modified tricarboxylic acid cycle". Nature. ج. 179 ع. 4568: 988–91. Bibcode:1957Natur.179..988K. DOI:10.1038/179988a0. PMID:13430766.
- ^ Capaldi R، Aggeler R (2002). "Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor". Trends Biochem Sci. ج. 27 ع. 3: 154–60. DOI:10.1016/S0968-0004(01)02051-5. PMID:11893513.
- ^ Opdenakker G، Rudd P، Ponting C، Dwek R (1993). "Concepts and principles of glycobiology". FASEB J. ج. 7 ع. 14: 1330–7. PMID:8224606.
- ^ McConville M، Menon A (2000). "Recent developments in the cell biology and biochemistry of glycosylphosphatidylinositol lipids (review)". Mol Membr Biol. ج. 17 ع. 1: 1–16. DOI:10.1080/096876800294443. PMID:10824734.
- ^ Chirala S، Wakil S (2004). "Structure and function of animal fatty acid synthase". Lipids. ج. 39 ع. 11: 1045–53. DOI:10.1007/s11745-004-1329-9. PMID:15726818.
- ^ Friedrich B، Schwartz E (1993). "Molecular biology of hydrogen utilization in aerobic chemolithotrophs". Annu Rev Microbiol. ج. 47: 351–83. DOI:10.1146/annurev.mi.47.100193.002031. PMID:8257102.
- ^ Weber K، Achenbach L، Coates J (2006). "Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction". Nat Rev Microbiol. ج. 4 ع. 10: 752–64. DOI:10.1038/nrmicro1490. PMID:16980937.
- ^ Dubey V، Bhalla R، Luthra R (2003). "An overview of the non-mevalonate pathway for terpenoid biosynthesis in plants" (PDF). J Biosci. ج. 28 ع. 5: 637–46. DOI:10.1007/BF02703339. PMID:14517367. مؤرشف من الأصل (PDF) في 2007-04-15.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Kuzuyama T، Seto H (2003). "Diversity of the biosynthesis of the isoprene units". Nat Prod Rep. ج. 20 ع. 2: 171–83. DOI:10.1039/b109860h. PMID:12735695.
- ^ Schroepfer G (1981). "Sterol biosynthesis". Annu Rev Biochem. ج. 50: 585–621. DOI:10.1146/annurev.bi.50.070181.003101. PMID:7023367.
- ^ Lees N، Skaggs B، Kirsch D، Bard M (1995). "Cloning of the late genes in the ergosterol biosynthetic pathway of Saccharomyces cerevisiae—a review". Lipids. ج. 30 ع. 3: 221–6. DOI:10.1007/BF02537824. PMID:7791529.
- ^ Strauss G، Fuchs G (1993). "Enzymes of a novel autotrophic CO2 fixation pathway in the phototrophic bacterium Chloroflexus aurantiacus, the 3-hydroxypropionate cycle". Eur J Biochem. ج. 215 ع. 3: 633–43. DOI:10.1111/j.1432-1033.1993.tb18074.x. PMID:8354269.
- ^ Wood H (1991). "Life with CO or CO2 and H2 as a source of carbon and energy". FASEB J. ج. 5 ع. 2: 156–63. PMID:1900793.
- ^ Ibba M، Söll D (2001). "The renaissance of aminoacyl-tRNA synthesis". EMBO Rep. ج. 2 ع. 5: 382–7. DOI:10.1093/embo-reports/kve095. PMC:1083889. PMID:11375928. مؤرشف من الأصل في 2011-05-01.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|deadurl=تم تجاهله (مساعدة) - ^ Lengyel P، Söll D (1969). "Mechanism of protein biosynthesis". Bacteriol Rev. ج. 33 ع. 2: 264–301. PMC:378322. PMID:4896351.
- ^ Rudolph F (1994). "The biochemistry and physiology of nucleotides". J Nutr. ج. 124 ع. 1 Suppl: 124S–127S. PMID:8283301. Zrenner R، Stitt M، Sonnewald U، Boldt R (2006). "Pyrimidine and purine biosynthesis and degradation in plants". Annu Rev Plant Biol. ج. 57: 805–36. DOI:10.1146/annurev.arplant.57.032905.105421. PMID:16669783.
- ^ Stasolla C، Katahira R، Thorpe T، Ashihara H (2003). "Purine and pyrimidine nucleotide metabolism in higher plants". J Plant Physiol. ج. 160 ع. 11: 1271–95. DOI:10.1078/0176-1617-01169. PMID:14658380.
- ^ Davies O، Mendes P، Smallbone K، Malys N (2012). "Characterisation of multiple substrate-specific (d)ITP/(d)XTPase and modelling of deaminated purine nucleotide metabolism". BMB Reports. ج. 45 ع. 4: 259–64. DOI:10.5483/BMBRep.2012.45.4.259. PMID:22531138.
- ^ Smith J (1995). "Enzymes of nucleotide synthesis". Curr Opin Struct Biol. ج. 5 ع. 6: 752–7. DOI:10.1016/0959-440X(95)80007-7. PMID:8749362.
- ^ "The biochemistry of drug metabolism—an introduction: part 1. Principles and overview". Chem Biodivers. ج. 3 ع. 10: 1053–101. 2006. DOI:10.1002/cbdv.200690111. PMID:17193224.
- ^ Danielson P (2002). "The cytochrome P450 superfamily: biochemistry, evolution and drug metabolism in humans". Curr Drug Metab. ج. 3 ع. 6: 561–97. DOI:10.2174/1389200023337054. PMID:12369887.
- ^ "UDP-glucuronosyltransferases". Curr Drug Metab. ج. 1 ع. 2: 143–61. 2000. DOI:10.2174/1389200003339171. PMID:11465080.
- ^ "Structure, function and evolution of glutathione transferases: implications for classification of non-mammalian members of an ancient enzyme superfamily". Biochem J. ج. 360 ع. Pt 1: 1–16. نوفمبر 2001. DOI:10.1042/0264-6021:3600001. PMID:11695986.
- ^ "Exploring the microbial biodegradation and biotransformation gene pool". Trends Biotechnol. ج. 23 ع. 10: 497–506. 2005. DOI:10.1016/j.tibtech.2005.08.002. PMID:16125262.
- ^ "Bacterial degradation of xenobiotic compounds: evolution and distribution of novel enzyme activities". Environ Microbiol. ج. 7 ع. 12: 1868–82. 2005. DOI:10.1111/j.1462-2920.2005.00966.x. PMID:16309386.
- ^ Davies K (1995). "Oxidative stress: the paradox of aerobic life". Biochem Soc Symp. ج. 61: 1–31. DOI:10.1042/bss0610001. PMID:8660387.
- ^ "Oxidative protein folding in eukaryotes: mechanisms and consequences". J Cell Biol. ج. 164 ع. 3: 341–6. 2004. DOI:10.1083/jcb.200311055. PMID:14757749.
- ^ Sies H (1997). "Oxidative stress: oxidants and antioxidants" (PDF). Exp Physiol. ج. 82 ع. 2: 291–5. DOI:10.1113/expphysiol.1997.sp004024. PMID:9129943.
- ^ "The antioxidants and pro-antioxidants network: an overview". Curr Pharm Des. ج. 10 ع. 14: 1677–94. 2004. DOI:10.2174/1381612043384655. PMID:15134565.
- ^ von Stockar U، Liu J (1999). "Does microbial life always feed on negative entropy? Thermodynamic analysis of microbial growth". Biochim Biophys Acta. ج. 1412 ع. 3: 191–211. DOI:10.1016/S0005-2728(99)00065-1. PMID:10482783.
- ^ Demirel Y، Sandler S (2002). "Thermodynamics and bioenergetics". Biophys Chem. ج. 97 ع. 2–3: 87–111. DOI:10.1016/S0301-4622(02)00069-8. PMID:12050002.
- ^ Albert R (2005). "Scale-free networks in cell biology". J Cell Sci. ج. 118 ع. Pt 21: 4947–57. arXiv:q-bio/0510054. DOI:10.1242/jcs.02714. PMID:16254242.
- ^ Brand M (1997). "Regulation analysis of energy metabolism". J Exp Biol. ج. 200 ع. Pt 2: 193–202. PMID:9050227.
- ^ "Signal transduction networks: topology, response and biochemical processes". J Theor Biol. ج. 238 ع. 2: 416–25. 2006. DOI:10.1016/j.jtbi.2005.05.030. PMID:16045939.
- ^ "Metabolic control". Essays Biochem. ج. 28: 1–12. 1994. PMID:7925313.
- ^ "Modern theories of metabolic control and their applications (review)". Biosci Rep. ج. 4 ع. 1: 1–22. 1984. DOI:10.1007/BF01120819. PMID:6365197.
- ^ Fell D، Thomas S (1995). "Physiological control of metabolic flux: the requirement for multisite modulation". Biochem J. ج. 311 ع. Pt 1: 35–9. PMC:1136115. PMID:7575476.
- ^ Hendrickson W (2005). "Transduction of biochemical signals across cell membranes". Q Rev Biophys. ج. 38 ع. 4: 321–30. DOI:10.1017/S0033583506004136. PMID:16600054.
- ^ Cohen P (2000). "The regulation of protein function by multisite phosphorylation—a 25 year update". Trends Biochem Sci. ج. 25 ع. 12: 596–601. DOI:10.1016/S0968-0004(00)01712-6. PMID:11116185.
- ^ Lienhard G، Slot J، James D، Mueckler M (1992). "How cells absorb glucose". Sci Am. ج. 266 ع. 1: 86–91. Bibcode:1992SciAm.266a..86L. DOI:10.1038/scientificamerican0192-86. PMID:1734513.
- ^ Roach P (2002). "Glycogen and its metabolism". Curr Mol Med. ج. 2 ع. 2: 101–20. DOI:10.2174/1566524024605761. PMID:11949930.
- ^ Newgard C، Brady M، O'Doherty R، Saltiel A (2000). "Organizing glucose disposal: emerging roles of the glycogen targeting subunits of protein phosphatase-1" (PDF). Diabetes. ج. 49 ع. 12: 1967–77. DOI:10.2337/diabetes.49.12.1967. PMID:11117996.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعSmithE - ^ Romano A، Conway T (1996). "Evolution of carbohydrate metabolic pathways". Res Microbiol. ج. 147 ع. 6–7: 448–55. DOI:10.1016/0923-2508(96)83998-2. PMID:9084754.
- ^ Koch A (1998). "How did bacteria come to be?". Adv Microb Physiol. Advances in Microbial Physiology. ج. 40: 353–99. DOI:10.1016/S0065-2911(08)60135-6. ISBN:978-0-12-027740-7. PMID:9889982.
- ^ Ouzounis C، Kyrpides N (1996). "The emergence of major cellular processes in evolution". FEBS Lett. ج. 390 ع. 2: 119–23. DOI:10.1016/0014-5793(96)00631-X. PMID:8706840.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعEbenhoh - ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعCascante - ^ Caetano-Anolles G، Kim HS، Mittenthal JE (2007). "The origin of modern metabolic networks inferred from phylogenomic analysis of protein architecture". Proc Natl Acad Sci USA. ج. 104 ع. 22: 9358–63. Bibcode:2007PNAS..104.9358C. DOI:10.1073/pnas.0701214104. PMC:1890499. PMID:17517598.
- ^ Schmidt S، Sunyaev S، Bork P، Dandekar T (2003). "Metabolites: a helping hand for pathway evolution?". Trends Biochem Sci. ج. 28 ع. 6: 336–41. DOI:10.1016/S0968-0004(03)00114-2. PMID:12826406.
- ^ Light S، Kraulis P (2004). "Network analysis of metabolic enzyme evolution in Escherichia coli". BMC Bioinformatics. ج. 5: 15. DOI:10.1186/1471-2105-5-15. PMC:394313. PMID:15113413.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) Alves R، Chaleil R، Sternberg M (2002). "Evolution of enzymes in metabolism: a network perspective". J Mol Biol. ج. 320 ع. 4: 751–70. DOI:10.1016/S0022-2836(02)00546-6. PMID:12095253. - ^ Kim HS، Mittenthal JE، Caetano-Anolles G (2006). "MANET: tracing evolution of protein architecture in metabolic networks". BMC Bioinformatics. ج. 7: 351. DOI:10.1186/1471-2105-7-351. PMC:1559654. PMID:16854231.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Teichmann SA، Rison SC، Thornton JM، Riley M، Gough J، Chothia C (2001). "Small-molecule metabolsim: an enzyme mosaic". Trends Biotechnol. ج. 19 ع. 12: 482–6. DOI:10.1016/S0167-7799(01)01813-3. PMID:11711174.
- ^ Spirin V، Gelfand M، Mironov A، Mirny L (يونيو 2006). "A metabolic network in the evolutionary context: Multiscale structure and modularity". Proc Natl Acad Sci USA. ج. 103 ع. 23: 8774–9. Bibcode:2006PNAS..103.8774S. DOI:10.1073/pnas.0510258103. PMC:1482654. PMID:16731630.
- ^ Lawrence J (2005). "Common themes in the genome strategies of pathogens". Curr Opin Genet Dev. ج. 15 ع. 6: 584–8. DOI:10.1016/j.gde.2005.09.007. PMID:16188434. Wernegreen J (2005). "For better or worse: genomic consequences of intracellular mutualism and parasitism". Curr Opin Genet Dev. ج. 15 ع. 6: 572–83. DOI:10.1016/j.gde.2005.09.013. PMID:16230003.
- ^ Pál C، Papp B، Lercher M، Csermely P، Oliver S، Hurst L (2006). "Chance and necessity in the evolution of minimal metabolic networks". Nature. ج. 440 ع. 7084: 667–70. Bibcode:2006Natur.440..667P. DOI:10.1038/nature04568. PMID:16572170.
- ^ Rennie M (1999). "An introduction to the use of tracers in nutrition and metabolism". Proc Nutr Soc. ج. 58 ع. 4: 935–44. DOI:10.1017/S002966519900124X. PMID:10817161.
- ^ Phair R (1997). "Development of kinetic models in the nonlinear world of molecular cell biology". Metabolism. ج. 46 ع. 12: 1489–95. DOI:10.1016/S0026-0495(97)90154-2. PMID:9439549.
- ^ Sterck L، Rombauts S، Vandepoele K، Rouzé P، Van de Peer Y (2007). "How many genes are there in plants (... and why are they there)?". Curr Opin Plant Biol. ج. 10 ع. 2: 199–203. DOI:10.1016/j.pbi.2007.01.004. PMID:17289424.
- ^ Borodina I، Nielsen J (2005). "From genomes to in silico cells via metabolic networks". Curr Opin Biotechnol. ج. 16 ع. 3: 350–5. DOI:10.1016/j.copbio.2005.04.008. PMID:15961036.
- ^ Gianchandani E، Brautigan D، Papin J (2006). "Systems analyses characterize integrated functions of biochemical networks". Trends Biochem Sci. ج. 31 ع. 5: 284–91. DOI:10.1016/j.tibs.2006.03.007. PMID:16616498.
- ^ Duarte NC، Becker SA، Jamshidi N، وآخرون (فبراير 2007). "Global reconstruction of the human metabolic network based on genomic and bibliomic data". Proc. Natl. Acad. Sci. U.S.A. ج. 104 ع. 6: 1777–82. Bibcode:2007PNAS..104.1777D. DOI:10.1073/pnas.0610772104. PMC:1794290. PMID:17267599.
- ^ Sterck L، Rombauts S، Vandepoele K، Rouzé P، Van de Peer Y (2007). "How many genes are there in plants (... and why are they there)?". Curr Opin Plant Biol. ج. 10 ع. 2: 199–203. DOI:10.1016/j.pbi.2007.01.004. PMID:17289424.
- ^ Borodina I، Nielsen J (2005). "From genomes to in silico cells via metabolic networks". Curr Opin Biotechnol. ج. 16 ع. 3: 350–5. DOI:10.1016/j.copbio.2005.04.008. PMID:15961036.
- ^ Ma HW، Zeng AP (2003). "The connectivity structure, giant strong component and centrality of metabolic networks". Bioinformatics. ج. 19 ع. 11: 1423–30. CiteSeerX:10.1.1.605.8964. DOI:10.1093/bioinformatics/btg177. PMID:12874056.
- ^ Zhao J، Yu H، Luo JH، Cao ZW، Li YX (2006). "Hierarchical modularity of nested bow-ties in metabolic networks". BMC Bioinformatics. ج. 7: 386. DOI:10.1186/1471-2105-7-386. PMC:1560398. PMID:16916470.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Ma HW، Zeng AP (2003). "The connectivity structure, giant strong component and centrality of metabolic networks". Bioinformatics. ج. 19 ع. 11: 1423–30. CiteSeerX:10.1.1.605.8964. DOI:10.1093/bioinformatics/btg177. PMID:12874056. González-Pajuelo M، Meynial-Salles I، Mendes F، Andrade J، Vasconcelos I، Soucaille P (2005). "Metabolic engineering of Clostridium acetobutylicum for the industrial production of 1,3-propanediol from glycerol". Metab Eng. ج. 7 ع. 5–6: 329–36. DOI:10.1016/j.ymben.2005.06.001. PMID:16095939. Krämer M، Bongaerts J، Bovenberg R، Kremer S، Müller U، Orf S، Wubbolts M، Raeven L (2003). "Metabolic engineering for microbial production of shikimic acid". Metab Eng. ج. 5 ع. 4: 277–83. DOI:10.1016/j.ymben.2003.09.001. PMID:14642355.
- ^ Zhao J، Yu H، Luo JH، Cao ZW، Li YX (2006). "Hierarchical modularity of nested bow-ties in metabolic networks". BMC Bioinformatics. ج. 7: 386. DOI:10.1186/1471-2105-7-386. PMC:1560398. PMID:16916470.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ Leroi, Armand Marie (2014). The Lagoon: How Aristotle Invented Science. Bloomsbury. ص. 400–401. ISBN:978-1-4088-3622-4.
{{استشهاد بكتاب}}: الوسيط غير المعروف|titlelink=تم تجاهله يقترح استخدام|وصلة العنوان=(مساعدة) - ^ Dr. Abu Shadi Al-Roubi (1982), "Ibn Al-Nafis as a philosopher", Symposium on Ibn al-Nafis, Second International Conference on Islamic Medicine: Islamic Medical Organization, Kuwait (cf. Ibn al-Nafis As a Philosopher, Encyclopedia of Islamic World [1])
- ^ Eknoyan G (1999). "Santorio Sanctorius (1561–1636) – founding father of metabolic balance studies". Am J Nephrol. ج. 19 ع. 2: 226–33. DOI:10.1159/000013455. PMID:10213823.
- ^ Williams, H. S. (1904) A History of Science: in Five Volumes. Volume IV: Modern Development of the Chemical and Biological Sciences Harper and Brothers (New York) Retrieved on 2007-03-26
- ^ Dubos J. (1951). "Louis Pasteur: Free Lance of Science, Gollancz. Quoted in Manchester K. L. (1995) Louis Pasteur (1822–1895)—chance and the prepared mind". Trends Biotechnol. ج. 13 ع. 12: 511–515. DOI:10.1016/S0167-7799(00)89014-9. PMID:8595136.
- ^ Kinne-Saffran E، Kinne R (1999). "Vitalism and synthesis of urea. From Friedrich Wöhler to Hans A. Krebs". Am J Nephrol. ج. 19 ع. 2: 290–4. DOI:10.1159/000013463. PMID:10213830.
- ^ Eduard Buchner's 1907 Nobel lecture at http://nobelprize.org Accessed 2007-03-20
- ^ Kornberg H (2000). "Krebs and his trinity of cycles". Nat Rev Mol Cell Biol. ج. 1 ع. 3: 225–8. DOI:10.1038/35043073. PMID:11252898.
- ^ Krebs HA، Henseleit K (1932). "Untersuchungen über die Harnstoffbildung im tierkorper". Z. Physiol. Chem. ج. 210: 33–66. DOI:10.1515/bchm2.1932.210.1-2.33.
Krebs H، Johnson W (أبريل 1937). "Metabolism of ketonic acids in animal tissues". Biochem J. ج. 31 ع. 4: 645–60. DOI:10.1042/bj0310645. PMC:1266984. PMID:16746382.
مزيد من القراءة
[عدل]تمهيدي
- Stryer, L. and (ردمك 0-7167-4955-6), The Chemistry of Life. (Penguin Press Science, 1999), Leroi, Armand Marie (2014). The Lagoon: How Aristotle Invented Science. Bloomsbury. صفحات 400–401. ISBN 978-1-4088-3622-4.Leroi, Armand Marie (2014). The Lagoon: How Aristotle Invented Science. Bloomsbury. ص. 400–401. ISBN:978-1-4088-3622-4.
- Nelson, D. L. and (ردمك 0-7167-4339-6), Into the Cool: Energy Flow, Thermodynamics, and Life. (University Of Chicago Press, 2005), "Metabolites: a helping hand for pathway evolution?". Trends Biochem Sci. ج. 28 ع. 6: 336–41. 2003. DOI:10.1016/S0968-0004(03)00114-2. PMID:12826406.
- "Network analysis of metabolic enzyme evolution in Escherichia coli". BMC Bioinformatics. ج. 5: 15. 2004. DOI:10.1186/1471-2105-5-15. PMID:15113413.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link), Oxygen: The Molecule that Made the World. (Oxford University Press, USA, 2004), Rennie M (2002). "Evolution of enzymes in metabolism: a network perspective". J Mol Biol. ج. 320 ع. 4: 751–70. DOI:10.1016/S0022-2836(02)00546-6. PMID:12095253.
متقدم
- Phair R (2006). "MANET: tracing evolution of protein architecture in metabolic networks". BMC Bioinformatics. ج. 7 ع. 12: 351. DOI:10.1186/1471-2105-7-351. PMID:16854231.
{{استشهاد بدورية محكمة}}: الوسيط|pages=و|page=تكرر أكثر من مرة (مساعدة)صيانة الاستشهاد: دوي مجاني غير معلم (link)الوسيط|pages=و|page=تكرر أكثر من مرة (مساعدة) and "Small-molecule metabolsim: an enzyme mosaic". Trends Biotechnol. ج. 19 ع. 12: 482–6. 2001. DOI:10.1016/S0167-7799(01)01813-3. PMID:11711174., Fundamentals of Enzymology: Cell and Molecular Biology of Catalytic Proteins. (Oxford University Press, 1999), "A metabolic network in the evolutionary context: Multiscale structure and modularity". Proc Natl Acad Sci USA. ج. 103 ع. 23: 8774–9. يونيو 2006. Bibcode:2006PNAS..103.8774S. DOI:10.1073/pnas.0510258103. PMID:16731630. - Williams, R. J. P. (ردمك 0-19-855598-9) and Lawrence J (2005). "Common themes in the genome strategies of pathogens". Curr Opin Genet Dev. ج. 15 ع. 6: 584–8. DOI:10.1016/j.gde.2005.09.007. PMID:16188434., Biochemistry. (W. H. Freeman and Company, 2002), Wernegreen J (2005). "For better or worse: genomic consequences of intracellular mutualism and parasitism". Curr Opin Genet Dev. ج. 15 ع. 6: 572–83. DOI:10.1016/j.gde.2005.09.013. PMID:16230003.
- "Chance and necessity in the evolution of minimal metabolic networks". Nature. ج. 440 ع. 7084: 667–70. 2006. Bibcode:2006Natur.440..667P. DOI:10.1038/nature04568. PMID:16572170. and "From genomes to in silico cells via metabolic networks". Curr Opin Biotechnol. ج. 16 ع. 3: 350–5. 2005. DOI:10.1016/j.copbio.2005.04.008. PMID:15961036., Lehninger Principles of Biochemistry. (Palgrave Macmillan, 2004), "Systems analyses characterize integrated functions of biochemical networks". Trends Biochem Sci. ج. 31 ع. 5: 284–91. 2006. DOI:10.1016/j.tibs.2006.03.007. PMID:16616498.
- "Global reconstruction of the human metabolic network based on genomic and bibliomic data". Proc. Natl. Acad. Sci. U.S.A. ج. 104 ع. 6: 1777–82. فبراير 2007. Bibcode:2007PNAS..104.1777D. DOI:10.1073/pnas.0610772104. PMID:17267599. "An introduction to the use of tracers in nutrition and metabolism". Proc Nutr Soc. ج. 58 ع. 4: 935–44. May 2007. Bibcode:2007PNAS..104.8685G. DOI:10.1017/S002966519900124X. PMID:10817161.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|year=لا يطابق|date=(مساعدة)تحقق من التاريخ في:|year= / |date= mismatch(مساعدة) "Development of kinetic models in the nonlinear world of molecular cell biology". Metabolism. ج. 46 ع. 12: 1489–95. July 2008. Bibcode:2008PNAS..105.9880L. DOI:10.1016/S0026-0495(97)90154-2. PMID:9439549.{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|year=لا يطابق|date=(مساعدة)تحقق من التاريخ في:|year= / |date= mismatch(مساعدة) and Eknoyan G (1999). "Santorio Sanctorius (1561–1636) – founding father of metabolic balance studies". Am J Nephrol. ج. 19 ع. 2: 226–33. DOI:10.1159/000013455. PMID:10213823., Brock's Biology of Microorganisms. (Benjamin Cummings, 2002), (ردمك 0-13-066271-2) - Da Silva, J.J.R.F. and "Bow ties, metabolism and disease". Trends Biotechnol. ج. 22 ع. 9: 446–50. 2004. DOI:10.1016/j.tibtech.2004.07.007. PMID:15331224., The Biological Chemistry of the Elements: The Inorganic Chemistry of Life. (Clarendon Press, 1991), "Louis Pasteur: Free Lance of Science, Gollancz. Quoted in Manchester K. L. (1995) Louis Pasteur (1822–1895)—chance and the prepared mind". Trends Biotechnol. ج. 13 ع. 12: 511–515. 1951. DOI:10.1016/S0167-7799(00)89014-9. PMID:8595136.
- "Vitalism and synthesis of urea. From Friedrich Wöhler to Hans A. Krebs". Am J Nephrol. ج. 19 ع. 2: 386. 1999. DOI:10.1159/000013463. PMID:10213830.
{{استشهاد بدورية محكمة}}: الوسيط|pages=و|page=تكرر أكثر من مرة (مساعدة)الوسيط|pages=و|page=تكرر أكثر من مرة (مساعدة) and "How many genes are there in plants (... and why are they there)?". Curr Opin Plant Biol. ج. 10 ع. 2: 199–203. 2007. DOI:10.1016/j.pbi.2007.01.004. PMID:17289424., Bioenergetics. (Academic Press Inc., 2002), "From genomes to in silico cells via metabolic networks". Curr Opin Biotechnol. ج. 16 ع. 3: 350–5. 2005. DOI:10.1016/j.copbio.2005.04.008. PMID:15961036.
"Metabolism". The Online Etymology Dictionary. اطلع عليه بتاريخ 2007-02-20.
روابط خارجية
[عدل]معلومات عامة
- The Biochemistry of Metabolism
- Sparknotes SAT biochemistry Overview of biochemistry. School level.
- MIT Biology Hypertextbook Undergraduate-level guide to molecular biology.
أيض الإنسان
- Topics in Medical Biochemistry Guide to human metabolic pathways. School level.
- http://themedicalbiochemistrypage.org/ THE Medical Biochemistry Page] Comprehensive resource on human metabolism.
قواعد بيانات
- Flow Chart of Metabolic Pathways at ExPASy
- IUBMB-Nicholson Metabolic Pathways Chart
- SuperCYP: Database for Drug-Cytochrome-Metabolism
مسارات أيضية
- Metabolism reference Pathway
- "Untersuchungen über die Harnstoffbildung im tierkorper". Z. Physiol. Chem. ج. 210 ع. 4: 33–66. 1932. DOI:10.1515/bchm2.1932.210.1-2.33. PMID:14642355.
[[تصنيف:أيض]] [[تصنيف:فسيولوجيا الغوص تحت الماء]]
