نزع النيتروجين
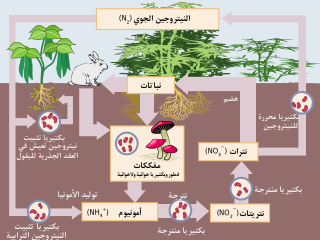
نزع النيتروجين[1] أو سَلْم النترجة[2] أو عكس النترجة[2] هو عملية إرجاع النترات بمساعدة الميكروبات (تؤديها مجموعة كبيرة من البكتيريا اللاهوائية الاختيارية غيرية التغذية) والتي يمكنها أن تنتج في النهاية نيتروجين جزيئي (N2) عن طريق سلسلة وسيطة من النواتج الغازية من أكاسيد الآزوت. ترجع هذه العملية التنفسية أكاسيد الآزوت كنتيجة لأكسدة مانح إلكترون مثل مادة عضوية. تشمل مستقبلات الإلكترون مرتبة حسب تفضيلها الديناميكي الحراري من الأكثر إلى الأقل: النترات (NO3−)، النتريت (NO2−)، أحادي أكسيد النيتروجين (NO)، أكسيد النيتروس (N2O) والتي تعطي بالنهاية ثنائي النيتروجين (N2) مكملة بذلك دورة النيتروجين. تتطلب ميكروبات نزع النيتروجين تراكيز منخفضة جداً من الأكسيجين أقل من 10%، إضافة إلى الكربون العضوي للطاقة. يمكن استخدام نزع النيتروجين لمعالجة مياه الصرف الصحي وفضلات الحيوانات ذات محتوى النيتروجين المرتفع، كونها تحد من تسرب NO3 إلى المياه الجوفية. كما يسمح نزع النيتروجين بإنتاج N2O، وهو من غازات الدفيئة التي تساهم بشكل ملحوظ في ارتفاع حرارة الأرض.
تتم العملية بشكل أساسي عن طريق بكتيريا غيرية التغذية (مثل Paracoccus denitrificans وعدة أنواع من الزوافات)،[3] تمَثل نازعات النيتروجين في كل مجموعة في علم الوراثة العرقي.[4] وتشارك عدة أنواع من البكتيريا في عملية الإرجاع الكامل للنترات إلى نيتروجين جزيئي، حيث تم التعرف على أكثر من مسار استقلابي في عملية الإرجاع.[5]
تعرف عملية الإرجاع المباشر للنترات إلى أمونيوم باسم إرجاع النترات إلى أمونيوم عن طريق التمثل العكسي[6] (بالإنجليزية: dissimilatory nitrate reduction to ammonium أو DNRA)، وهي ممكنة عند الأحياء التي تملك[7] جين-nrf، ولكنها أقل شيوعاً من عملية نزع النيتروجين في معظم الأنظمة الطبيعية التي يتم فيها إرجاع النترات. تملك أنواع أخرى من الأحياء الميكروبية التي تقوم بعملية الإرجاع جينات (nir: nitrite reductase) و (nos: nitrous oxide reductase) وغيرها؛[4] ومن بين الأحياء التي تملك هذاه الجينات Alcaligenes faecalis و Alcaligenes xylosoxidans و Bradyrhizobium japonicum و Blastobacter denitrificans وكثير من الزوافات.[8]
محددات التغذية
[عدل]تتطلب كافة الأحياء توافر مواد مغذية في محيطها لضمان بقائها.[9] وغالباً ما يكون النيتروجين هو عامل التغذية المحدد للنمو، يأتي بعده الفوسفور كعامل رئيسي آخر ويتفاعل هذين العاملين كيميائياً.[10] يمكن لبعض الأحياء نزع النيتروجين والفوسفور.[11] الرابطة الثلاثية في N2 تجعله شديد الاستقرار؛ لذا تعتمد معظم الأحياء (كالنباتات) على بعضها لتكسير هذه الرابطة وتحويلها إلى شكل يمكن الاستفادة منه في التفاعلات الحيوية.[12] انظر النترجة. العلاقة التعايشية بين أنواع المستجذرات و البقل موثقة بشكل جيد.[13]
الشروط المطلوبة
[عدل]تخضع عملية نزع النيتروجين إلى شروط خاصة في الأنظمة البيئية البحرية والبرية.[12] وبشكل عام فإنها تحدث عندما يستنفذ الأكسيجين؛ فهو مستقبل إلكترون مفضل طاقياً، وتتنفس البكتيريا النترات كمستقبل إلكترون بديل طرفي. بسبب وفرة تراكيز عالية من الأكسيجين في الغلاف الجوي فإنها تحدث فقط في البيئات التي ينقص فيها الأكسيجين، حيث يكون استهلاك الأكسيجين أكبر من تزويده وحيث تتواجد كميات كافية من النترات. هذه البيئات تشمل أتربة محددة[14] و المياه الجوفية،[15] و المناطق الرطبة و خزانات الزيت[16] والزوايا سيئة التهوية من المحيط ورواسب قعر البحر.
يتم نزع النيتروجين بشكل عام عن طريق مزيج من الأشكال الوسيطة التالي:
- NO3− → NO2− → NO + N2O → N2 (غاز)
يمكن التعبير عن العملية الكاملة لنزع النيتروجين كتفاعل إرجاع:
- 2 NO3− + 10 e− + 12 H+ → N2 + 6 H2O
يبدي التفاعل تجزئة في تركيب النظائر. حيث يفضل هذا التفاعل نظائر النيتروجين الأخف، تاركاًَ النظائر الأثقل في المادة المتبقية. يمكن أن تعطي العملية قيم-دلتا تصل إلى -40، حيث تمثل دلتا الفرق بين تركيب النظائر. ويمكن استخدامه لتمييز عمليات نزع النيتروجين في الطبيعة.
الاستخدام المتعمد للعملية
[عدل]يستخدم نزع النيتروجين بشكل شائع في إزالة النيتروجين من الصرف الصحي ومياه الصرف المحلي. وهي عملية مفيدة في المناطق الرطبة[17] وعلى الضفاف[18] لإزالة الزائد من النترات في المياه الجوفية الناجمة عن الاستخدام الزراعي أو السكني المفرط للأسمدة.[19]
يمكن أن يتم التفاعل في ظروف نقص الأكسيجين عن طريق عملية تدعى الأكسدة اللاهوائية للأمونيا (بالإنجليزية: anammox):[20]
- NH4+ + NO2− → N2 + 2 H2O
تضاف كميات قليلة من الميثانول أو الإيثانول أو الخلات أو الجليسرول أو بعض المنتجات ذات الملكية الخاصة (ماركة مسجلة) في بعض معامل معالجة مياه الصرف لتوفير مصدر للكربون لبكتيريا نزع النيتروجين.[21] كما تستخدم عملية نزع النيتروجين في معالجة النفايات الصناعية.[22]
أثرها على تغير المناخ العالمي
[عدل]تؤثر زيادة معدلات ثنائي أكسيد الكربون في الغلاف الجوي على دورة التغذية، لكن يصعب التنبؤ بهذه الآثار.[23] ستتأثر التفاعلات الكيميائية بين التربة والجو بتغير التركيبة الجوية.[24] هناك دلائل تشير إلى أن زيادة تسميد التربة تؤدي إلى التقليل من احتباس الكربون.[25]
لقد تبين أن الجداول والأنهار التي تصلها كميات من النيتروجين الناجمة عن استخدام الأراضي السكنية والزراعية هي مصدر هام من مصادر أكسيد النيتروس في الغلاف الجوي.[26]
انظر أيضاً
[عدل]مراجع
[عدل]- ^ المعجم الموحد لمصطلحات علم الأحياء، سلسلة المعاجم الموحدة (8) (بالعربية والإنجليزية والفرنسية)، تونس: مكتب تنسيق التعريب، 1993، OCLC:929544775، QID:Q114972534
- ^ ا ب إدوار غالب (1988). الموسوعة في علوم الطبيعة: تبحث في الزراعة والنبات والحيوان والجيولوجيا (بالعربية واللاتينية والألمانية والفرنسية والإنجليزية) (ط. 2). بيروت: دار المشرق. ج. 2. ص. 805. ISBN:978-2-7214-2148-7. OCLC:44585590. OL:12529883M. QID:Q113297966.
- ^ Carlson, C. A., and J. L. Ingraham. 1983. Comparison of denitrification by Pseudomonas stutzeri, Pseudomonas aeruginosa, and Paracoccus denitrificans. Appl. Environ. Microbiol. 45:1247-1253.
- ^ ا ب Zumft, W. 1997. Cell biology and molecular basis of denitrification. Microbiol. Mol. Biol. Rev. 61:533-616.
- ^ Atlas, R.M., Barthas, R. Microbial Ecology: Fundamentals and Applications. 3rd Ed. Benjamin-Cummings Publishing. ISBN 0-8053-0653-6
- ^ An, S., and W. S. Gardner. 2002. Dissimilatory nitrate reduction to ammonium (DNRA) as a nitrogen link, versus denitrification as a sink in a shallow estuary (Laguna Madre/Baffin Bay, Texas). Marine Ecology Progress Series 237:41-50.
- ^ Spanning, R., M. Delgado, and D. Richardson. 2005. "It is possible to encounter DNRA when your source of carbon is a fermentable substrate, as glucose, so if you wanna avoid DNRA use a non fermentable substrate. The Nitrogen Cycle: Denitrification and its Relationship to N2 Fixation, p. 277-342."
- ^ Liu, X., S. M. Tiquia, G. Holguin, L. Wu, S. C. Nold, A. H. Devol, K. Luo, A. V. Palumbo, J. M. Tiedje, and J. Zhou. 2003. Molecular Diversity of Denitrifying Genes in Continental Margin Sediments within the Oxygen-Deficient Zone off the Pacific Coast of Mexico. Appl. Environ. Microbiol. 69:3549-3560
- ^ Howarth, R. W. 1988. Nutrient Limitation of Net Primary Production in Marine Ecosystems. Annual Review of Ecology and Systematics 19:89-110.
- ^ Vance, C. P. 2001. Symbiotic Nitrogen Fixation and Phosphorus Acquisition. Plant Nutrition in a World of Declining Renewable Resources. Plant Physiol. 127:390-397.
- ^ Kuba, T., M. C. M. Van Loosdrecht, F. A. Brandse, and J. J. Heijnen. 1997. Occurrence of denitrifying phosphorus removing bacteria in modified UCT-type wastewater treatment plants. Water Research 31:777-786.
- ^ ا ب Seitzinger, S., J. A. Harrison, J. K. Bohlke, A. F. Bouwman, R. Lowrance, B. Peterson, C. Tobias, and G. V. Drecht. 2006. Denitrification Across Landscapes and Waterscapes: A Synthesis. Ecological Applications 16:2064-2090.
- ^ Daniel, R. M., I. M. Smith, J. A. D. Phillip, H. D. Ratcliffe, J. W. Drozd, and A. T. Bull. 1980. Anaerobic Growth and Denitrification by Rhizobium japonicum and Other Rhizobia. J Gen Microbiol 120:517-521.
- ^ Scaglia، J.؛ Lensi، R.؛ Chalamet، A. (1985). "Relationship between photosynthesis and denitrification in planted soil". Plant and Soil. ج. 84 ع. 1: 37–43. DOI:10.1007/BF02197865.
- ^ Korom، Scott F. (1992). "Natural Denitrification in the Saturated Zone: A Review". Water Resources Research. ج. 28 ع. 6: 1657–1668. Bibcode:1992WRR....28.1657K. DOI:10.1029/92WR00252.
- ^ Cornish Shartau، S. L.؛ Yurkiw، M.؛ Lin، S.؛ Grigoryan، A. A.؛ Lambo، A.؛ Park، H. S.؛ Lomans، B. P.؛ Van Der Biezen، E.؛ Jetten، M. S. M.؛ Voordouw، G. (2010). "Ammonium Concentrations in Produced Waters from a Mesothermic Oil Field Subjected to Nitrate Injection Decrease through Formation of Denitrifying Biomass and Anammox Activity". Applied and Environmental Microbiology. ج. 76 ع. 15: 4977–4987. DOI:10.1128/AEM.00596-10. PMC:2916462. PMID:20562276.
- ^ Bachand, P. A. M., and A. J. Horne. 1999. Denitrification in constructed free-water surface wetlands: II. Effects of vegetation and temperature. Ecological Engineering 14:17-32.
- ^ Martin, T. L., N. K. Kaushik, J. T. Trevors, and H. R. Whiteley. 1999. Review: Denitrification in temperate climate riparian zones. Water, Air, and Soil Pollution 111:171-186.
- ^ Mulvaney, R. L., S. A. Khan, and C. S. Mulvaney. 1997. Nitrogen fertilizers promote denitrification. Biology and Fertility of Soils 24:211-220.
- ^ Dalsgaard, T., B. Thamdrup, and D. E. Canfield. 2005. Anaerobic ammonium oxidation (anammox) in the marine environment. Research in Microbiology 156:457-464.
- ^ Chen, K.-C., and Y.-F. Lin. 1993. The relationship between denitrifying bacteria and methanogenic bacteria in a mixed culture system of acclimated sludges. Water Research 27:1749-1759.
- ^ Constantin, H., and M. Fick. 1997. Influence of C-sources on the denitrification rate of a high-nitrate concentrated industrial wastewater. Water Research 31:583-589.
- ^ Sinclair, T. R. 1992. Mineral Nutrition and Plant Growth Response to Climate Change. J. Exp. Bot. 43:1141-1146.
- ^ Rosenzweig, C., and D. Hillel. 2000. Soils and Global Climate Change: Challenges and Opportunities. Soil Science 165:47-56.
- ^ Oren, R., D. S. Ellsworth, K. H. Johnsen, N. Phillips, B. E. Ewers, C. Maier, K. V. R. Schafer, H. McCarthy, G. Hendrey, S. G. McNulty, and G. G. Katul. 2001. Soil fertility limits carbon sequestration by forest ecosystems in a CO2-enriched atmosphere. Nature 411:469-472.
- ^ "New study focuses on nitrogen in waterways as cause of nitrous oxide in the atmosphere". مؤرشف من الأصل في 2017-09-14.
