هكسازينون
| هكسازينون | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
3-Cyclohexyl-6-(dimethylamino)-1-methyl-1,3,5-triazine-2,4(1H,3H)-dione |
|
| أسماء أخرى | |
فيلبار |
|
| المعرفات | |
| رقم التسجيل (CAS) | 51235-04-2 |
| بب كيم (PubChem) | 39965 |
|
|
|
|
| الخواص | |
| الصيغة الجزيئية | C12H20N4O2 |
| الكتلة المولية | 252.31 |
| المظهر | بلورات صلبة بيضاء اللون |
| الكثافة | 1.25 جرام/سم3 |
| نقطة الانصهار | 116 °س، 389 °ك، 241 °ف |
| الذوبانية في الماء | قابل للذوبان |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
الهكسازينون هو مركب عضوي يستخدم كمبيد للأعشاب على نطاق واسع، ويوجد على صورة مادة صلبة عديمة اللون.
يُظهر الهكسازينون بعض القابلية للذوبان في الماء، ولكنه قابل للذوبان بدرجة عالية في معظم المذيبات العضوية باستثناء الألكانات. ويُعد الهكسازينون أحد مكونات مبيدات الأعشاب التي تنتمي إلى فئة التريازينات. تصنع شركة دو بونت للكيماويات مُركب الهكسازينون، وتبيعه تحت الاسم التجاري فيلبار.[1]
يعمل الهكسازينون عن طريق تثبيط التمثيل الضوئي ومن ثم فهو مبيد أعشاب غير انتقائي. يستخدم الهكسازينون للتحكم في نمو الحشائش والنباتات العشبية عريضة الأوراق، والنباتات الخشبية. يستخدم نحو 33٪ تقريبًا من إجمالي ما يُستهلك في الولايات المتحدة الأمريكية من مبيد الهكسازينون في زراعة البرسيم، ونحو 31٪ منه في الغابات، وحوالي 29٪ منه في المناطق الصناعية، و4٪ منه في المروج الطبيعية والمراعي، ويستخدم ما يقل عن 2٪ منه في زراعة قصب السكر.[2]
يُعد مركب الهكسازينون ملوثاً عضويًا منتشراً في المياه الجوفية بسبب ارتفاع قابليته للذوبان في الماء.
لمحة تاريخية
[عدل]يستخدم الهكسازينون على نطاق واسع كمبيد للأعشاب، وهو مبيد أعشاب غير انتقائي ينتمي إلى عائلة التريازينات، ويمكن استخدامه في مجموعة واسعة من الأماكن.
يستخدم الهكسازينون للتحكم في الأعشاب الضارة في جميع أنواع البيئات بدءًا من مزارع قصب السكر، والمشاتل الميدانية للغابات، ومزارع الأناناس، ووصولاً إلى الحشائش العالية، والسكك الحديدية، ومواقع المصانع الصناعية.[3]
استُخدم الهكسازينون لأول مرة في عام 1975 للمكافحة الشاملة للأعشاب الضارة، ثم أعقب ذلك استخدامه في المحاصيل الزراعية.[4]
البنية والتفاعلات
[عدل]يمكن أن ترتبط مبيدات الأعشاب التي تنتمي إلى فئة التريازينات مثل الهكسازينون ببروتين D-1 كينون لسلسلة نقل الإلكترون في النظام الضوئي الثاني لتثبيط عملية التمثيل الضوئي، وبالتالي يمكن لهذه الإلكترونات المنحرفة أن تدمر الأغشية وتدمر الخلايا النباتية.[5]
التحضير
[عدل]يمكن تحضير الهكسازينون من خلال عمليتي تفاعل مختلفتين. تبدأ إحدى عمليات تحضير الهكسازينون بتفاعل كلوروفورمات الميثيل مع السياناميد، لتكوين الهكسازينون بعد سلسلة تفاعلات من خمس خطوات كما يلي:[6]
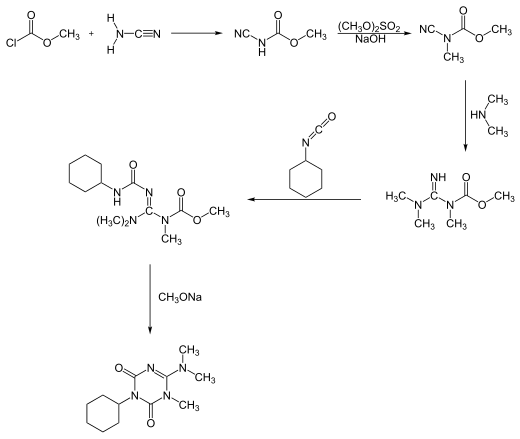
أما العملية الثانية فتبدأ من ثيويوريا الميثيل كما هو موضح:[6]
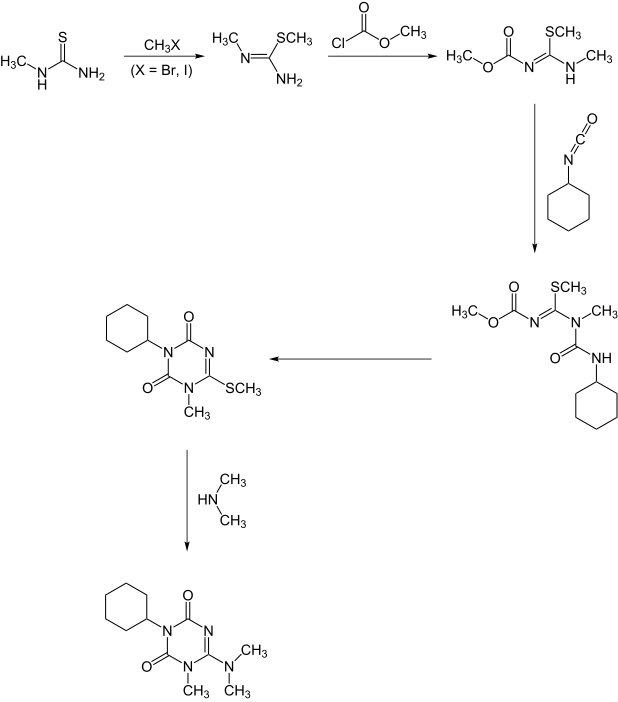
انحلال
[عدل]خضع موضوع انحلالية الهكسازينون للدراسة على مدى سنوات طويلة،[7] ووجد أنه يتحلل بنسبة 10٪ تقريبًا في غضون خمسة أسابيع عند تعرضه لأشعة الشمس الاصطناعية في الماء المقطر. ويمكن أن تكون انحلالية الهكسازينون في المياه الطبيعية أكبر بثلاث إلى سبع مرات. والأمر المثير للدهشة هو أن كلا من الأس الهيدروجيني ودرجة حرارة الماء لا يؤثران بشكل كبير على التحلل الضوئي للهكسازينون.[8] يتحلل الهكسازينون بشكل رئيسي عن طريق الكائنات الحية الدقيقة الهوائية في التربة.[9]
آلية العمل
[عدل]يُعد الهكسازينون مبيد أعشاب واسع الطيف ومتبقي، إذا تمتصه الأوراق والجذور بسرعة، كما يمكن أن تتحمله النباتات التي تنتمي إلى فصيلة الصنوبريات، لذا فهو مبيد أعشاب فعال للغاية لمكافحة الحشائش عريضة الأوراق السنوية والدائمة، وبعض الأعشاب، وبعض الأنواع الخشبية.
يعمل الهكسازينون بشكل جيد في الأجواء والغابات المطيرة، لأن الأمطار أو ذوبان الجليد يجعلان مبيدات الأعشاب تتحرك إلى أسفل في التربة حيث تمتص الجذور الهكسازينون من التربة،[10] ثم ينتقل الهكسازينون عبر الأنسجة الموصلة إلى الأوراق، حيث يمنع التمثيل الضوئي للنبات داخل البلاستيدات الخضراء. كما يرتبط الهكسازينون بأحد بروتينات مركب النظام الضوئي الثاني، والذي يمنع نقل الإلكترون. وهو الأمر الذي ينجم عنه ردود الفعل المتعددة التالية:
يتفاعل الكلوروفيل ذو الحالة الثلاثية الأول مع الأكسجين لتكوين الأكسجين الأحادي.
يقوم كل من الكلوروفيل والأكسجين الأحادي بعد ذلك بإزالة أيونات الهيدروجين من الدهون غير المشبعة الموجودة في الخلايا والأغشية العضية، وتشكيل الجذور الدهنية.
تعمل هذه الجذور على أكسدة الدهون والبروتينات الأخرى، مما يؤدي في النهاية إلى فقدان سلامة غشاء الخلايا والعضيات، وهو ما سيؤدي بدوره إلى فقدان الكلوروفيل، وتسرب المحتويات الخلوية، وموت الخلايا، ثم موت النبات في نهاية المطاف.[11]
تظهر النباتات الخشبية في البداية اصفرار الأوراق قبل أن تبدأ أوراقها في التساقط، ثم تموت في النهاية.[12] في بعض الأحيان تكون النباتات قادرة على إعادة نمو الأوراق والتساقط مرة أخرى خلال موسم النمو.
المراجع
[عدل]- ^ Arnold P. Appleby, Franz Müller, Serge Carpy "Weed Control" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. دُوِي:10.1002/14356007.a28_165
- ^ Hexazinone, Herbicide Profile, Pesticide Management Education Program, جامعة كورنيل نسخة محفوظة 2020-02-25 على موقع واي باك مشين.
- ^ Wang، Huili؛ Xu، Shuxia؛ Tan، Chengxia؛ Wang، Xuedong (30 مايو 2009). "Anaerobic biodegradation of hexazinone in four sediments". Journal of Hazardous Materials. ج. 164 ع. 2–3: 806–811. DOI:10.1016/j.jhazmat.2008.08.073. PMID:18824297.
- ^ "Hexazinone: Reregistration Eligibility Decision (RED) Fact Sheet" (PDF). مؤرشف من الأصل (PDF) في 2021-12-12.
- ^ "Agronomy 317 - Iowa State University". agron-www.agron.iastate.edu. مؤرشف من الأصل في 2016-11-23. اطلع عليه بتاريخ 2017-03-15.
- ^ ا ب Ullmann's agrochemicals. Wiley-VCH. 1 يناير 2007. ISBN:9783527316045. OCLC:470787466.
- ^ Helling، C. S.؛ Kearney، P. C.؛ Alexander، M. (1971). "Behavior of pesticides in soil". Adv. Agron. Advances in Agronomy. ج. 23: 147–240. DOI:10.1016/S0065-2113(08)60153-4. ISBN:9780120007233.
- ^ Rhodes، R. C. (1980b). "Studies with 14C-labeled hexazinone in water and bluegill sunfish". J. Agric. Food Chem. ج. 28 ع. 2: 306–310. DOI:10.1021/jf60228a002. PMID:7391368.
- ^ Rhodes، R. C. (1980a). "Soil Studies with 14C-labeled hexazinone". J. Agric. Food Chem. ج. 28 ع. 2: 311–315. DOI:10.1021/jf60228a012.
- ^ Ghassemi، M.؛ وآخرون (1981). Environmental fates and impacts of major forest use pesticides. Washington D.C. ص. 169–194.
{{استشهاد بكتاب}}: صيانة الاستشهاد: مكان بدون ناشر (link) - ^ "Weed Science Society of America". wssa.net (بالإنجليزية الأمريكية). Archived from the original on 2022-05-01. Retrieved 2017-03-15.
- ^ Sidhu، S. S.؛ Feng.، J. C. (1993). "Hexazinone and its metabolites in boreal forest vegetation". Weed Sci. ج. 41 ع. 2: 281–287. DOI:10.1017/S0043174500076177.

