بنتاسين
| بنتاسين | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
Pentacene |
|
| المعرفات | |
| رقم CAS | 135-48-8 |
| بوب كيم (PubChem) | 8671 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | C22H14 |
| الكتلة المولية | 278.36 غ/مول |
| المظهر | صلب أزرق/أسود اللون |
| الكثافة | 1.3 غ/سم3 |
| نقطة الانصهار | 271 °س (يتسامى عند 372 °س) |
| الذوبانية في الماء | عملياً غير منحل في الماء |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
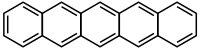
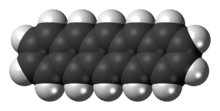
بنتاسين هو هيدروكربون عطري متعدد الحلقات يتألف من خمس حلقات بنزين مندمجة مع بعضها بشكل خطّي (أسين) وبأسلوب مترافق. ينتمي المركب بنيوياً إلى مجموعة الأسينات؛ ويعد من أشباه الموصلات العضوية، ويكون على شكل صلب أزرق/أسود اللون له بريق قرمزي.
تمكن باحثون من شركة آي بي إم في سنة 2009 من نشر نتائج تجارب مخبرية تتضمن صور لجزيء منفرد من البنتاسين حصل عليها باستخدام مجهر القوة الذرية؛[3][4] حيث صور الباحثون ذرات كربون قطر الواحدة منها 0.14 نانومتر، واستنبطوا مواقع ذرات الهيدروجين في الجزيء من الصورة المأخوذة له.[5] وفي سنة 2011، تم استخدام تقنية معدلة من مجهر المسح النفقي لتحديد شكل أعلى مدار جزيئي مشغول/أدنى مدار جزيئي غير مشغول تجريبياً.[6][7]

التحضير
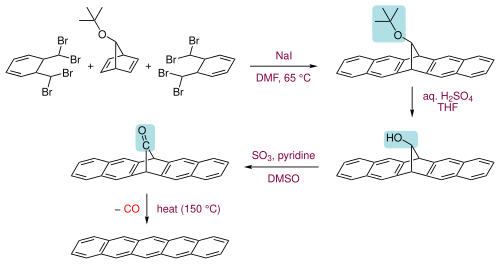
[عدل]يحضر البنتاسين نموذجياً من تفاعل إيلبس Elbs reaction. كما يمكن أن تتم عملية التحضير في المختبر من بنتاسين-13,6-ديون أو بنتاسين-14,5-ديون، ثم بإجراء عملية اختزال أو بثق لجزيء أحادي أكسيد الكربون عند درجات حرارة حوالي 150 °س.[9] يحصل على بنتاسين-13,6-ديون بعدة طرق، منها إجراء تفاعل تكاثف بين جزيئي ثنائي ألدهيد مع هيدروكينون.[10]
هناك عدة استرتيجيات لتحضير مركب البنتاسين ومشتقاته.
الخواص
[عدل]يوجد البنتاسين على شكل بلورت زرقاء داكنة مسودة، تتبع في بنيتها البلورية النظام البلوري الثلاثي.[11]
يولّد أكسيتونات عند التعرّض للأشعة فوق البنفسجية (UV) أو الضوء المرئي، مما يجعله حساساً جداً للأكسدة. لهذا السبب فإنه يتفكك عند التعرض للهواء أو الضوء.
الاستخدامات
[عدل]هناك العديد من التطبيقات لمركب البنتاسين ومشتقاته في مجال التقنية الإلكترونية.
يستخدم البنتاسين كشبه موصل في الإلكترونيات العضوية؛[12] وذلك غالباً على هيئة ترانزستور ذو مفعول حقلي عضوي (OFET).
وجد في سنة 2012 أن مركب بارا-تيرفينيل المطعّم بالبنتاسين فعّال كوسط مضخم للميزر عند درجة حرارة الغرفة.[13]
المراجع
[عدل]- ^ ا ب ج PENTACENE (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ "Single molecule's stunning image". BBC News. 28 أغسطس 2009. مؤرشف من الأصل في 2019-05-13. اطلع عليه بتاريخ 2009-08-28.
- ^ Gross, L.؛ Mohn، F؛ Moll، N؛ Liljeroth، P؛ Meyer، G (2009). "The Chemical Structure of a Molecule Resolved by Atomic Force Microscopy". Science. ج. 325 ع. 5944: 1110–4. Bibcode:2009Sci...325.1110G. DOI:10.1126/science.1176210. PMID:19713523.
- ^ "إنجاز يهيئ لثورة حاسوبية". الجزيرة. 1/9/2009. مؤرشف من الأصل في 13 ديسمبر 2019. اطلع عليه بتاريخ 07-02-2017.
{{استشهاد بخبر}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ Krieger, K. (23 أغسطس 2011). "Molecules Imaged Most Intimately". Science Now. مؤرشف من الأصل في 2011-12-21.
{{استشهاد بخبر}}: استعمال الخط المائل أو الغليظ غير مسموح:|ناشر=(مساعدة) - ^ Gross, L.؛ Moll, N.؛ Mohn, F.؛ Curioni, A.؛ Meyer, G.؛ Hanke, F.؛ Persson, M. (2011). "High-Resolution Molecular Orbital Imaging Using a p-Wave STM Tip". Phys. Rev. Lett. ج. 107 ع. 8: 86101–86104. Bibcode:2011PhRvL.107h6101G. DOI:10.1103/PhysRevLett.107.086101. PMID:21929180.
- ^ Dinca، L. E.؛ De Marchi، F.؛ MacLeod، J. M.؛ Lipton-Duffin، J.؛ Gatti، R.؛ Ma، D.؛ Perepichka، D. F.؛ Rosei، F. (2015). "Pentacene on Ni(111): Room-temperature molecular packing and temperature-activated conversion to graphene". Nanoscale. ج. 7 ع. 7: 3263–9. DOI:10.1039/C4NR07057G. PMID:25619890.
- ^ Chen, Kew-Yu؛ Hsieh، HH؛ Wu، CC؛ Hwang، JJ؛ Chow، TJ (2007). "A new type of soluble pentacene precursor for organic thin-film transistors". Chemical Communications ع. 10: 1065–7. DOI:10.1039/b616511g. PMID:17325807.
- ^ Q. Miao, M. Lefenfeld, T.-Q. Nguyen, T. Siegrist, C. Kloc, C. Nuckolls: Self-Assembly and Electronics of Dipolar Linear Acenes. In: Adv. Mater. Band 17, Nr. 4, 2005, S. 407–412, (Details der chemischen Synthese sind in den Supporting Informations beschrieben.).
- ^ Theo Siegrist u. a. (2001). "Enhanced Physical Properties in a Pentacene Polymorph". Angewandte Chemie International Edition. ج. 40 ع. 9: 1732–1736. DOI:10.1002/1521-3773(20010504)40:9<1732::AID-ANIE17320>3.0.CO;2-7.
- ^ Hagen Klauk (Hrsg.): Organic Electronics: Materials, Manufacturing and Applications. Wiley-VCH Verlag, Weinheim 2006, ISBN 3-527-31264-1.
- ^ Brumfiel، G. (2012). "Microwave laser fulfills 60 years of promise". Nature. DOI:10.1038/nature.2012.11199.